Al-Mg-Si 합금에서 열처리가 열확산도와 부식특성에 미치는 영향
Influences of Heat Treatment on the Thermal Diffusivity and Corrosion Characterization of Al-Mg-Si alloy
Article information
Trans Abstract
The effect of the heat treatment on the Mg2Si phase in Al-Mg-Si alloy was investigated by a laser flash apparatus (LFA), Differential scanning calorimetry (DSC) and corrosion test. The alloy samples were solution treated at 590 °C for a half hour followed by warm water quenching, and then aged in air at 180, 200 and 240 °C for 5 hours. The results showed that the corrosion resistance of the solid solution treated sample was more improved than the as cast sample. Aging treatment also helped increase corrosion resistance at room temperature. It is thought that the fine Mg2Si precipitation phase on the grain had a more positive effect on improving corrosion resistance than crystallization of the Mg2Si phase on the grain boundaries. Corrosion rate also decreased with increasing aging treatment. The corrosion rate of AT240 was reduced to 1.16 MPY compared with the AT180 test piece, which had a corrosion rate of 3.79 MRY. The solution treated sample also showed lower thermal diffusivity than the aged samples. The thermal diffusivity increased as the solute concentration of Mg and Si in the a-Al matrix rapidly decreased during aging treatment. On the other hand, the thermal diffusivity of the aged samples, in which precipitation was completed by the aging process, decreased as the temperature rose. The thermal conductivities of all samples were similar near 250 °C when the β'' phase and β' precipitation was completed.
1. 서 론
최근 에너지 효율에 대한 관심이 증가하며, 해수 환경에서 사용 가능한 열 교환기의 재료로 스테인리스와 구리를 대체할 수 있는 Al 합금에 대한 연구가 관심을 받고 있다 [1-3]. Al 합금은 스테인리스와 구리에 비해 가격이 저렴하고 가볍다는 장점이 있으며, 스테인리스에 비해 열전도도가 높다. 열전도도와 열 방출 속도의 관계를 정리한 푸리에 방정식(식 1)에 따르면, 열전도도가 높은 재료는 열의 방출 속도가 우수하여 열 교환기용 재료로 사용하기에 적합하다.
여기서 q는 방출되는 열의 유속 또는 열의 밀도, k는 열전도도, ∇T는 온도 차이를 의미한다. 또한 Al 합금은 내부식성이 좋고, 대기 조건에서 부동태 피막에 의한 고내부식성을 갖는다. Al 합금의 부동태 피막은 첨가 원소에 따라 내부식성이 달라지는 것으로 알려져 있다 [4,5]. Al 합금 중 내부식성이 우수한 Mg를 포함한 Al-Mg 합금이나 Al-Mg-Si 합금이 주로 부식 환경에서 많이 사용된다.
Al-Mg-Si 합금에서 대표 적인 금속간 화합물인 Mg2Si상은 합금의 물리적/기계적 특성에 주요한 영향을 미치는 것으로 알려져 있다 [6,7]. Mg2Si상은 Mg과 Si이 원자비 2:1로 결합하여 형성되며, 용체화 및 시효 처리를 통해 고용 및 석출 반응을 제어할 수 있다. 용체화 처리에 의해 고용된 Mg2Si상은 Mg와 Si원자로 분해되어 Al 기지에 고용되어 있다가 시효 처리에 의해 석출 된다 [8-10]. 석출된 Mg2Si상은 안정상으로 성장하기 전 다양한 중간상(G.P. zone, β”, β’, β 등)의 형태를 거치며, 석출상의 크기, 기지 조직과의 정합 여부에 따라 합금의 물리적/기계적 특성에 주요한 영향을 미친다 [8,11]. 그래서 많은 연구자들이 Mg2Si상의 석출 및 분해가 합금 특성에 미치는 영향에 대해 연구하고 있다 [12-14]. 그러나, 열처리에 의한상의 석출이 합금의 내부식성 및 열전도도 성능에 어떠한 영향을 미치는지 연구한 사례는 거의 없다. 따라서 본 연구에서는 Mg2Si상을 포함하는 Al-Mg-Si 합금을 열처리 하여 부식 환경에서 Mg2Si상이 내부식성에 미치는 영향을 연구하였다. 또한 열 교환기에 중요한 특성인 열 방출 효과를 확인하기 위해 석출상이 고온 열확산도에 미치는 영향을 조사하였다.
2. 시험 방법
2.1 합금 제조 및 열처리
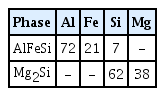
연구에 사용한 Al-Mg-Si 합금은 99.97% 공업용 순 Al, 98.5% 순도의 Si 펠릿, 99.9% 순도의 Mg 잉곳을 이용하여 중력주조로 제조하였다. 합금 성분은 Mg와 Si의 반응비와 열처리 중 Al에 고용가능한 Mg2Si 량을 고려하여 1.9 wt%의 Mg2Si의 함량을 갖도록 설계하였다. 주조 중 산화물과 수소가스를 제거하기 위한 탈 가스 처리(gas bubbling filtration, GBF)는 99.9% Ar 가스를 사용하여 750 °C에서 15분 동안 실시하였다. 탈가스 처리된 용탕은 15분간 안정화 후 95(± 5)°C로 예열된 금형에 주조하여 잉곳을 제작하였다. 주조한 Al-Mg-Si 합금의 자세한 성분은 표 1에 나타내었다. 제조된 Al-Mg-Si 합금의 용체화 처리는 590 °C에서 30분 동안 실시하고, 80 °C 물에 급랭하였다. 과고용체 상태의 합금은 각 각 180, 200, 240 °C에서 5시간 동안 시효 처리 되었다.
미세조직 관찰용 시편은 SiC와 다이아몬드 서스펜션으로 경면 연마 후 0.1% NaOH 수용액으로 에칭하여 준비하였다. 각 시편은 광학현미경을 이용하여 미세조직을 관찰하였으며, 정출상 및 석출상의 성분 분석은 EDX를 활용하여 분석하였다.
열량분석은 Mg2Si상의 석출 반응 및 반응 온도를 확인하기 위해 실시하였으며, 열 유속(heat flux)형 시차주사 열량계(Differential scanning calorimetry, DSC)를 사용하였다. 열량분석용 시편은 지름 6 mm, 두께 1 mm로 준비하였다. DSC 분석은 백금-라듐 합금 도가니에 시편을 넣고 상온에서 530 °C 까지 10 °C/min 속도로 스캔하며 열량 변화를 측정하였다. 가열로 내 분위기는 고순도 질소 가스(99.999%)로 유지하였으며, 표준 시편은 비어있는 백금-라듐 도가니를 사용하였다.
동전위 분극시험은 각 시편의 부식전위와 부식전류밀도 등을 비교하기 위해 실시하였다. 기준전극으로는 포화 칼로메 전극(SCE)을 사용하고 보조전극(Count electrode)은 고밀도 탄소봉을 사용하였다. 분극 시험에 사용된 모든 시편은 SiC paper #1200의 조도로 연마하여 동일한 표면을 갖도록 하였다. 동전위 분극시험은 2.5% NaCl 수용액을 사용하여 상온에서 개방전위 안정성을 확보한 후 5 mV/sec의 속도로 분석하였다.
Al 합금의 열전도도에 대한 평가는 열확산도 값으로 비교하였다. 열전도도는 열확산도, 비열, 밀도의 곱으로 계산된다. 열확산도를 제외한 비열과 밀도는 물리적 값으로 Al 성분에 따라 변화하지 않는다는 특성이 있다. 그러나, 열확산도는 금속의 미세조직이나 구조에 따라 영향을 받으므로, 동종 합금에서 열처리에 의한 열전도도를 결정하는 중요한 인자로 작용한다. 각 시료의 열확산도는 섬광법(laser flash analysis, LFA)을 이용하여 측정하였다. 열확산도 시편은 지름 12.7 mm, 두께 2.5 mm로 제작하였다. 측정 중 시편과 장비의 산화를 막기 위해 분위기는 고순도 질소(99.999% N2) 상태로 유지하였다.
3. 결과 및 고찰
3.1 미세조직 분석
주조 공정으로 제작한 Al-1.9%Mg2Si 합금의 열처리 전과 후 미세조직을 관찰하여 그림 1에 나타내었다. 그림 1(a)에서 주조 공정 중 정출된 Mg2Si상과 AlFeSi 3원계 금속간 화합물이 결정립을 따라 존재하고 있음을 볼 수 있다. 주조 응고 시 고순도 α-Al상이 먼저 응고된 후 합금 원소 들은 결정립에 고립되어 정출된다 [15]. 주조 시편을 590 °C에서 용체화 처리 한 후 급랭하면 그림 1(b)와 같은 조직이 나타난다. 용체화 처리로 인해 Mg2Si상은 Al 기지에 고용되기 때문에 조직 사진에서는 AlFeSi상만 관찰된다. 용체화 후 AlFeFi상은 얇고 긴 침상 형태로 결정립을 따라 존재하였다. 그림 1(c)의 용체화 처리 후 240 °C, 5시간 동안 시효 처리 시편에서는 결정립 내에 미세한 Mg2Si상이 석출된 것을 확인 할 수 있다. 주조 시편의 결정립에 존재하던 Mg2Si상이 용체화 및 시효 처리를 통해 결정 내부에서 석출되었다는 사실을 알 수 있다. 각 정출 상의 세부 성분은 표 2와 같다.
3.2 열처리에 따른 Mg2Si상 석출 거동 분석
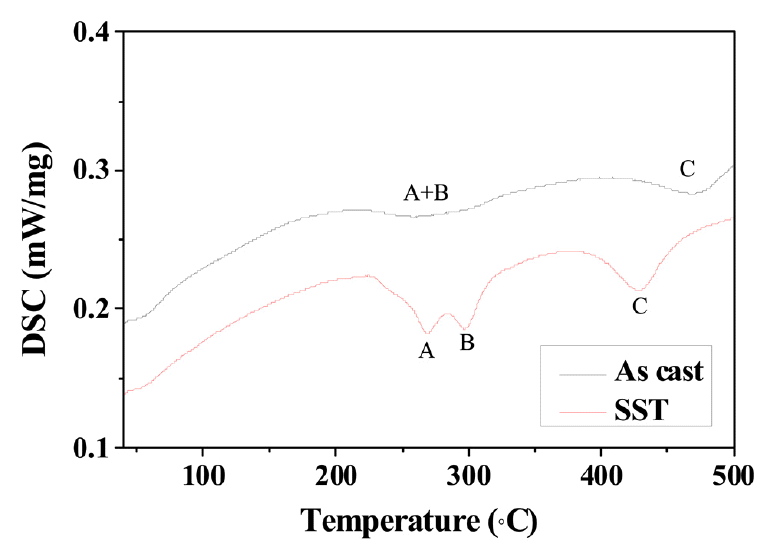
용체화 처리에 따른 Mg2Si의 용해는 시차주사열량분석을 통해서도 확인할 수 있다. 용체화 전과 후 시편에 대해 시차주사열량분석을 실시하고 그 결과로 얻은 열량분석곡선을 그림 2에 나타냈다. Al-Mg-Si 시편의 주조 시편과 용체화 시편의 열 흐름 곡선에서 유사한 반응 온도와 다른 크기를 가지는 발열 곡선과 흡열 곡선이 관찰되었다. 그 중 석출을 의미하는 발열 곡선에 대해 A, B, C로 명명하였다. 열 흐름 곡선은 금속재료가 가열될 때 발생하는 상의 석출과 용해 반응을 유추할 수 있도록 도와준다. Mg와 Si이 포함된 Al 합금에서 Mg2Si상의 석출과 성장은 온도에 따라 단계적으로 발생하며, 그 순서는 다음과 같다 [10,16].
과포화고용체 (SSS) → G.P. zone → β” → β’ → β (Mg2Si)
이러한 Mg2Si 중간상의 석출 및 성장 반응에 따른 나타나는 발열 반응은 많은 연구를 통해 일정한 온도 구간에서 발생하는 것으로 보고되고 있다. 기존의 연구를 참고로 그림 2에 나타난 A 곡선은 β”상의 석출, B 곡선은 β’상 석출, C 곡선은 β상 석출에 의해 발생함을 알 수 있다 [13,17,18]. 열 흐름 곡선에서 발열 곡선의 면적은 석출 반응의 엔탈피와 같으며, 면적이 넓을수록 많은 양의 석출 반응이 진행되었음을 의미한다 [19-21]. Mg2Si 양이 같은 동일 합금에서 발열 곡선의 면적이 달라지는 것은 기지 내부에 고용되어 있는 용질량 차이 때문이다. 용체화 시편의 열 흐름 곡선과 비교하여 주조 시편의 열 흐름 곡선에서 A와 B 반응이 연속되어 나타났는데, 이는 주조 상태는 용체화 처리를 하지 않아 G.P. Zone 형성의 구동력(driving force)이 낮고, 초기 석출 반응이 중첩되어 발생했기 때문이다.
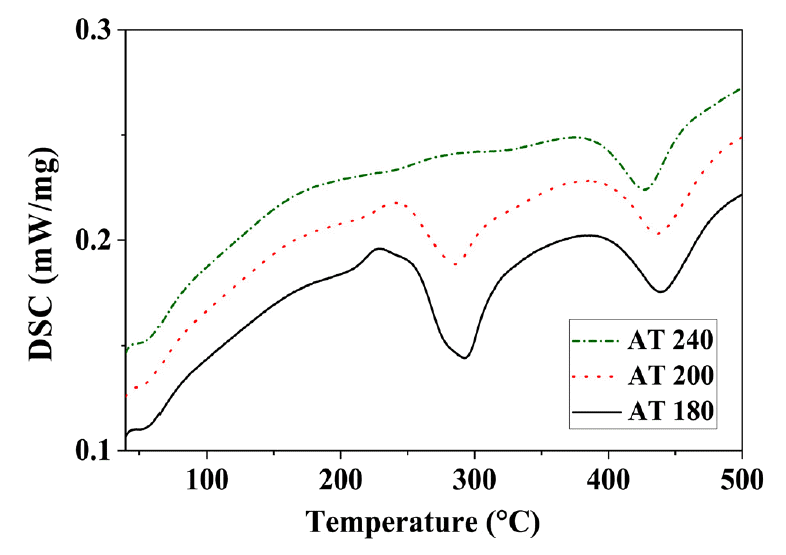
용체화 처리 후 Mg2Si 석출을 위한 시효 처리를 실시하고, 각 조건에 따른 석출량 및 석출상을 비교하기 위해 시차주사열량분석을 실시하였다. 각 시효 조건에 따른 열 흐름 곡선은 그림 3에 나타내었다. 그림 2에서 나타낸 용체화 시편의 열 흐름 곡선과 비교하면, 시효온도가 증가함에 따라 A, B 곡선의 크기는 감소하는 경향을 보인다. AT180과 AT200 시편의 경우 A와 B에 해당하는 2개의 곡선이 중첩되어 하나로 나타났고, AT240 시편에서는 A+B 곡선이 관찰되지 않았다. 앞서 언급 한 바와 같이 발열 곡선의 넓이는 석출량과 비례하므로, 발열 곡선의 크기가 시효온도 증가에 따라 감소하는 것은 시효 처리 중 Mg2Si의 석출량이 증가하였음을 의미한다. 특히, AT240의 열 흐름 곡선에서 A+B 곡선이 관찰되지 않는 것은 시효 처리 중 β”상과 β’상의 석출이 완료된 것으로 해석할 수 있다.
3.3 열처리에 따른 Mg2Si상 변화가 부식성에 미치는 영향
용체화 처리가 부식 반응에 미치는 영향을 알아보기 위해 주조 시편과 용체화 시편을 동전위 분극시험 한 결과를 그림 4에 나타냈다. 그림 4에서 확인된 주조 시편의 부식 전위는 -1.53V, 용체화 시편의 부식 전위는 -1.52V이다. 타펠 분석을 통해 계산된 주조 시편의 최대 부식 전류 밀도는 4.57 × 10-6 A/cm2으로, 용체화 처리 된 시편의 최대 부식 전류 밀도 6.33 × 10-6 A/cm2 보다 낮다. 부식 전위와 최대 부식 전류 밀도를 비교하여 주조 시편에 비해 용체화 처리 된 시편의 내부식성이 더 높다는 사실을 알 수 있다. Al-Mg-Si 합금에서 Mg2Si상은 Al 기지와 갈바닉 쌍을 이룰 때 양극으로 작용하여 Mg2Si상 주변의 Al을 부식시킨다. 용체화 처리는 입계에 존재하던 정출된 Mg2Si상의 분율을 감소시켰고, 분해된 Mg2Si상은 모재에 고용되어 있음을 앞선 그림 1(b)와 그림 2에서 각각 확인 할 수 있다. 즉, 용체화 처리를 통해 부식 반응에 참여할 수 있는 Mg2Si상 분율이 감소하여 합금의 내부식성이 향상 된 것으로 보인다 [10,22-24].
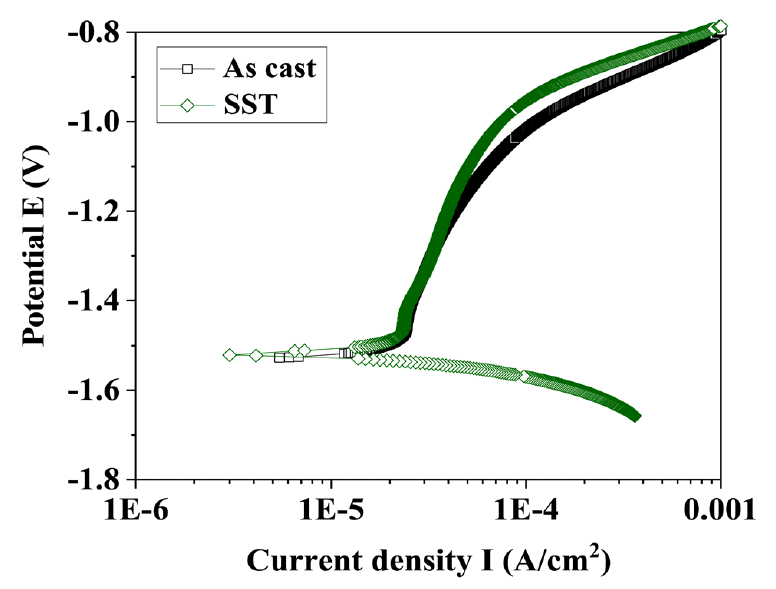
Potentiodynamic polarization curves of studied alloy samples for before and after solid solution treatment
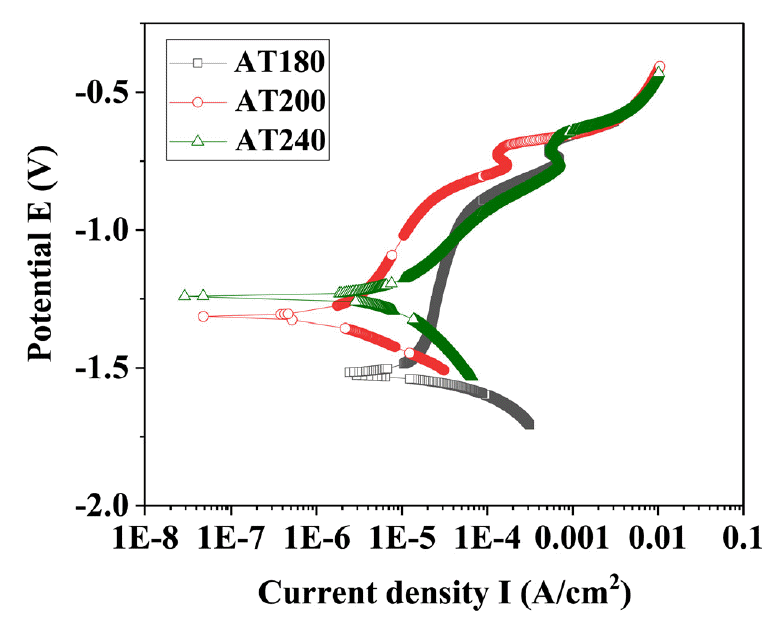
각 시효 조건에 따른 합금의 내부식성 평가를 위해 동전위 분극시험을 실시하고 그 결과를 그림 5에 나타내었다. 또한 각 시편의 최대부식전류밀도와 부식속도를 그림 6에 정리하였다. 시효 온도가 180, 200, 240 °C로 증가하면서 분극전위는 양의 방향으로 이동하여 시효가 진행될수록 부식전위가 감소하였다. 최대부식전류밀도 역시 시효 온도가 증가할수록 감소하여 합금의 내부식성이 증가하는 것을 알 수 있다. 부식속도는 AT180 시편이 3.79 MRY로 가장 빠르고, AT240 시편은 1.16 MPY로 AT180 시편 대비 약 1/2 이하의 부식속도를 가진다. 그림 3의 열 흐름 곡선에 따르면 시효 온도가 높아질수록 Mg2Si상의 석출 속도가 증가하였는데, 이는 내부식성의 향상과 비례관계를 갖는다. 또한, β”상과 β’상 석출이 거의 완료된 AT240 시편도 내부식성이 가장 높게 나타났다. 이를 통해 시효 온도의 증가와 그로 인한 석출물의 성장은 합금의 내부식성에 긍정적인 영향을 미치는 것으로 판단된다. 특히, 그 효과는 β” 상과 β’상 석출이 완료된 AT240 시편에서 가장 높게 나타났다. 주조 시편에서 Mg2Si상이 결정립계에 존재하면 양극으로 작용하기 때문에 모재의 부식을 촉진한다는 기존 연구들과 달리 [7,25], 본 연구에서는 입내에 석출하는 미세한 Mg2Si상이 합금의 내부식성을 향상시키는데 기여한 것으로 보인다.
3.4 열처리에 따른 Mg2Si상 변화와 열확산도
열처리를 통한 Mg2Si상의 고용과 석출은 합금의 열확산도에도 영향을 미친다. 그림 7은 주조 직 후와 용체화 처리한 Al-1.9Mg2Si 합금의 열확산도를 측정한 결과이다. 앞에서 용체화 처리로 모재 내에 고용된 Mg2Si상은 내부식성을 향상시키는 효과가 있었으나, 열확산도 측면에서는 부정적 효과를 나타냈다. 상온에서 주조 시편의 상온열확산도는 81.9 mm/s2에서 용체화 처리 후 67.4 mm/s2로 급격히 감소하였다. 상온에서 열확산도 차이가 발생하는 원인은 그림 2의 열 흐름 곡선의 A, B피크로 나타난 β”상과 β’상의 고용량의 영향으로 보인다. 앞서 언급했듯이 용체화 시편의 열량분석에서 β”상과 β’상 석출량이 많다는 것은 용체화 시편 내부에 고용된 용질량이 많았다는 것을 의미한다. Mg2Si상이 열처리 중 Al 기지에 고용되면, Mg와 Si는 원자 단위로 Al 격자 사이에 존재한다 [5]. 이러한 첨가 원소 원자들은 Al 격자에 변형을 야기하며 동시에 자유전자 이동을 방해하게 된다. 금속과 같이 자유전자를 갖는 재료에서 열은 자유 전자와 포논을 열 전달체로 삼아 이동하는데, 그 경로에 존재하는 첨가 원소나 결함 등은 열의 이동을 방해하는 저항으로 작용한다 [28-30]. 따라서 기지를 통해 이동하는 열 전달체의 수가 감소하게 되어 열의 이동이 어려워지고 결과적으로 열확산도가 감소하게 된다. 한편 주조 시편은 상대적으로 느린 응고 속도로 인해 그림 1의 미세조직과 같이 Mg2Si상이 입계에 정출되어 존재하며 열 흐름 곡선에 따르면 고용된 용질의 양도 상대적으로 적어 열확산도가 높은 것으로 보인다.
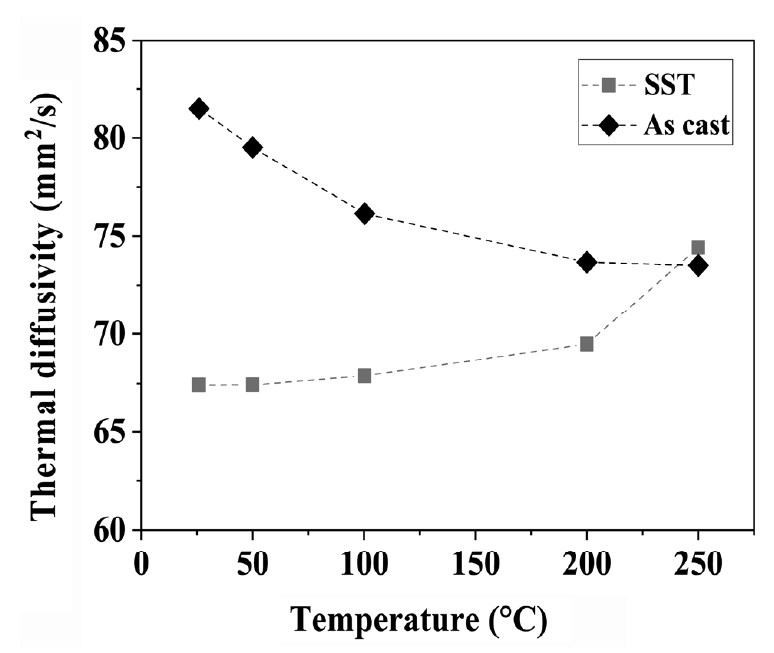
Temperature dependence of the thermal diffusivity of the studied alloy before and after solid solution treatment
한편, 분석 온도 상승에 따라 두 시편의 열확산도는 서로 다른 경향으로 변화한다. 주조 시편의 열확산도는 온도 증가에 따라 감소하나, 용체화 시편의 상승하는 거동을 보였다. 용체화 시편은 열의 유입으로 인해 고용된 용질이 석출하기 때문에 그림 2에서 보여주는 Mg2Si상의 석출 거동에 비례하여 열확산도가 증가한다. 반대로 주조 시편은 Mg2Si를 비롯한 정출상들이 온도 증가에 따라 고용도가 증가하여 재 고용되며, 동시에 온도 증가에 따라 포논의 활성화로 열 전달이 방해 받기 때문이다.
온도 별 시효 처리에 따른 Al-1.9Mg2Si 합금의 열확산도를 측정한 결과는 그림 8과 같다. AT180 시편의 상온 열확산도는 69.1 mm/s2로 용체화 시편에 비해 약 1.7 mm/s2 증가하였다. 시효 온도가 높아질수록 열확산도 증가 폭도 증가하여, AT200 시편의 상온 열확산도는 79.7 mm/s2로 용체화 시편에 비해 10 mm/s2 이상 높은 열확산도는 갖는다. AT240 시편은 열 흐름 곡선에서 Mg2Si상의 석출이 대부분 완료된 상태로 확인되었으며 상온에서 높은 열확산도를 가진다. 그러나 분석 온도가 증가하면서 AT240 시편의 열확산도는 하락하는 경향을 보인다. 온도가 증가하면서 포논에 의한 열 저항이 증가하는 동시에 더 이상 석출에 의한 열확산도 증가는 나타나지 않기 때문에 결과적으로 열확산도는 감소한다. 한편, 열 흐름 곡선 결과에서 석출반응이 완료되지 않았던 SST, AT180 시편은 상온 열확 산도는 낮으나, 온도가 증가하는 경우에도 열확산도가 하락하지 않는다. 석출이 완료되지 않은 합금들은 고온에서 포논의 열 전달 방해로 인한 열확산도 감소 효과와 석출로 인한 열 저항 감소로 인한 열확산도 향상 효과가 상쇄되어 온도 증가에도 불구하고 열확산도가 일정하게 유지되는 구간이 존재한다. 일반적으로 시효 처리 중 Al 격자에 흩어져 있던 합금 원소들이 집합체를 형성하고 성장하면서 Al 기지에 존재하는 열 저항 인자가 감소하면서 열확산도 하락이 억제된다 [26,27].
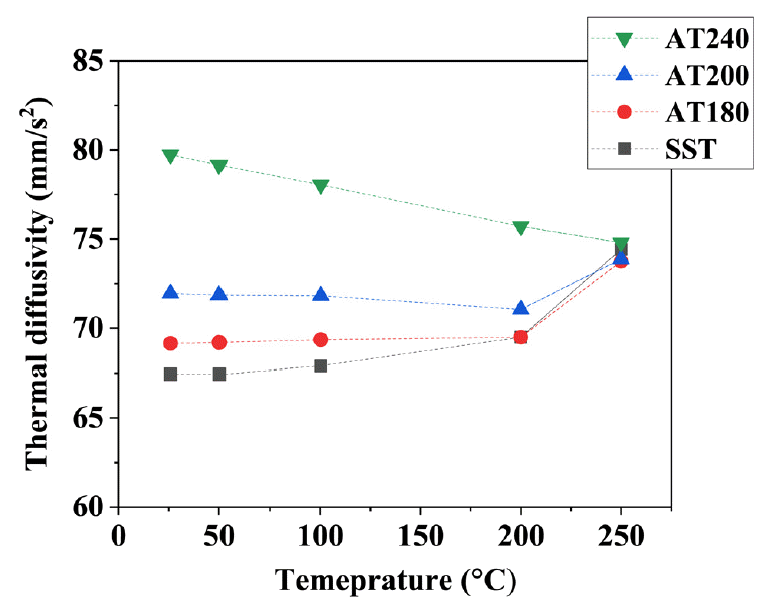
Temperature dependence of the thermal diffusivity of the studied alloy after various aging treatments.
그림 7과 8에서 각 시편의 열확산도가 250 °C에서 유사한 값으로 수렴하는 것을 볼 수 있다. 이 온도는 그림 2와 3의 열 흐름 곡선에서 β”상과 β’상의 석출 온도와 유사하다. 250 °C에서 발생하는 β"상과 β’상 석출이 마무리 되면서 모든 시편의 열확산도는 같아지게 되는데, 이러한 경향은 β상의 석출 여부와는 큰상관이 없었다. 즉, Al-Mg-Si 합금에서 Mg2Si상의 석출에 의한 열확산도의 증가는 안정상인 β상의 석출 보다는 준안정상인 β”상과 β’상의 석출에 의한 영향이 지배적인 것으로 보인다.
4. 결 론
Al-Mg-Si 합금에서 열처리를 통한 Mg2Si상 제어가 부식 및 열확산도의 관계에 대해 연구하였고 다음과 같은 결론을 얻을 수 있었다.
1. Al-Mg-Si 합금에서 용체화 처리 시 분해되는 Mg2Si는 내부식성 향상에 긍정적인 영향을 주었다. 이는 Al과 갈바닉 쌍을 이루는 Mg2Si가 기지에 고용되면서 부식에 참여할 확률이 낮아지기 때문이다. 그러나 AlFeSi상의 잔류와 기지의 불안정으로 인해 그 효과가 크게 나타나지는 않았다.
2. 시효 온도가 증가할수록 Mg2Si상의 석출양은 증가하며, 내부식성도 함께 향상되어 AT240 시편이 가장 우수한 부식 저항성을 가진다. 동일한 Mg2Si 함량에도 불구하고 입계에 정출된 Mg2Si상 보다 입내에 석출하는 미세한 Mg2Si상이 내부식성에 더 긍정적인 영향을 미친다.
3. 상온 열확산도는 시효 온도가 높은 AT240에서 79.7 mm/s2 로 가장 우수하며, 용체화 시편에서 69.1 mm/s2로 가장 낮다. 그러나 온도가 상승할수록 AT240 시편의 열확산도는 감소하고 용체화 시편은 증가하여 250 °C에서 모든 시편의 열확산도는 같아졌다.
4. 연구에서 사용된 Al-1.9Mg2Si 합금은 용체화 후 240 °C 시효 처리 한 경우 β”상과 β’상의 석출이 완료되었으며, 이때 가장 우수한 내부식성 및 열확산도를 갖는 것으로 확인되었다.
Acknowledgements
이 성과는 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(No. 2021R1F1A1049962).