1. ņä£ ļĪĀ
Zr-2.5%Nb ĒĢ®ĻĖłņØĆ Ļ│Āņś© Ļ░ĢļÅä, ļé┤ņŗØņä▒, ņżæņä▒ņ×É ĒØĪņłś ļŗ©ļ®┤ņĀü ĒŖ╣ņä▒ņØ┤ ņÜ░ņłśĒĢśņŚ¼ ņżæņłśļĪ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļĪ£ ņé¼ņÜ®ļÉ£ļŗż [1]. Zr-2.5%Nb ĒĢ®ĻĖł ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļŖö ╬▒+╬▓ ņśüņŚŁņØĖ 850 ┬░CņŚÉņä£ ņÜ®ņ▓┤ĒÖö ņ▓śļ”¼ Ēøä, Ļ│Āņś© ņĢĢņČ£ (hot extrusion)Ļ│╝ ļāēĻ░ä ņØĖļ░£ Ļ│ĄņĀĢņ£╝ļĪ£ ņĀ£ņĪ░ļÉ£ļŗż [2,3]. ĻĘĖ Ēøä ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļŖö 400 ┬░CņŚÉņä£ 24ņŗ£Ļ░ä ņØæļĀź ņĀ£Ļ▒░ ņ▓śļ”¼ļź╝ ĒĢ£ļŗż. As-received ņāüĒā£ņØś ļ»ĖņäĖņĪ░ņ¦üņØĆ ╬▓-Zr ņāüņØĆ ╬▒-Zr ņāü ņé¼ņØ┤ņØś Ļ│äļ®┤ņŚÉ ļČäĒżĒĢ£ļŗż. ╬▒-ZrņØĆ 90% ņĀĢļÅäņØś ļČĆĒö╝ ļČäņ£©ņØä Ļ░Ćņ¦Ćļ®░, 10% ņĀĢļÅäņØś ļČĆĒö╝ ļČäņ£©ņØä Ļ░¢ļŖö ╬▓-ZrņØĆ ņĢĮ 20% ņĀĢļÅäņØś Nbļź╝ ĒĢ©ņ£ĀĒĢśĻ│Ā ņ׳ļŗż.
ņżæņłśļĪ£ ņĢĢļĀźĻ┤ĆņØĆ ņøÉņ×ÉļĪ£ Ļ░ĆļÅÖ ņżæ ļāēĻ░üņ×¼ņØĖ D2OĻ░Ć ĒØÉļź┤ļŖö ņ£ĀļĪ£ļź╝ ņĀ£Ļ│ĄĒĢśņŚ¼ ņøÉņ×ÉļĪ£ 1ņ░© Ļ▓ĮĻ│äļź╝ ĒśĢņä▒ĒĢ£ļŗż[4]. ņĀĢņāü ņÜ┤ņĀä ņŗ£ ļāēĻ░üņ×¼ ņś©ļÅäļŖö ņ×ģĻĄ¼ ņĖĪņŚÉņä£ 260 ┬░C ņĀĢļÅäņØ┤Ļ│Ā ņČ£ĻĄ¼ ņĖĪņŚÉņä£ 310 ┬░C ņĀĢļÅäņØ┤ļŗż. ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś Zr ņøÉņåīļŖö D2OņÖĆ ļ░śņØæĒĢśņŚ¼ ZrO2Ļ░Ć ĒśĢņä▒ļÉśĻ│Ā ņżæņłśņåī(D, deuterium) ņøÉņ×ÉĻ░Ć ļ░£ņāØĒĢśņŚ¼ ņĢĢļĀźĻ┤Ć ļé┤ļČĆļĪ£ ĒØĪņłśļÉ£ļŗż. Ļ░ĆļÅÖ ņĢĢļĀźĻ┤ĆņØś ņ┤Ø ņłśņåī ļåŹļÅäļŖö ņĀ£ņĪ░ Ļ│ĄņĀĢņŚÉņä£ ņ£Āņ×ģļÉ£ ņ┤łĻĖ░ ņłśņåīņŚÉ Ļ░ĆļÅÖ ņżæ ĒØĪņłśļÉ£ ņżæņłśņåīņØś ĒĢ®ņ£╝ļĪ£ ņĀĢņØśļÉ£ļŗż.
ņĢĢļĀźĻ┤ĆņŚÉ ņ╣©Ēł¼ļÉśļŖö ņżæņłśņåī ņ¢æņØĆ ņĢĢļĀźĻ┤ĆņØś ņ£äņ╣śņŚÉ ļö░ļØ╝ ļŗżļź┤ļŗż [5]. ņżæņłśņåī ņ╣©Ēł¼ ņ£©(ingress rate)ņØĆ ņĢĢļĀźĻ┤ĆņØś roll jointņŚÉ Ļ░ĆĻ╣īņÜ┤ inlet ļ░Å outlet ļČĆņ£äĻ░Ć ļŗżļźĖ Ļ││ļ│┤ļŗż Ēø©ņö¼ ļŹö ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż. ņĢĢļĀźĻ┤ĆņŚÉ ĒØĪņłśļÉ£ ņ┤Ø ņłśņåīĻ░Ć Ļ│ĀņÜ® ĒĢ£ļÅä ņØ┤ļé┤ņØ╝ ļĢīļŖö ņÖäņĀäĒ׳ Ļ│ĀņÜ®ļÉśĻ│Ā, Ļ│ĀņÜ®ĒĢ£ļÅäļź╝ ļäśņ£╝ļ®┤ ņłśņåīĒÖöļ¼╝ļĪ£ ņäØņČ£ĒĢ£ļŗż [6]. ņĢĢļĀźĻ┤ĆņØĆ Ļ░ĆļÅÖ ņ┤łĻĖ░ņŚÉļŖö ņłśņåī ļåŹļÅäĻ░Ć ļé«ņĢä ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ļÉśņ¦Ć ņĢŖņ£╝ļéś, Ļ░ĆļÅÖ ĻĖ░Ļ░äņØ┤ ĻĖĖņ¢┤ņ¦Ćļ®┤ inletņØ┤ļéś outlet ļČĆņ£äņŚÉņä£ Ļ│ĀņÜ®ĒĢ£ļÅäļź╝ ļäśņ¢┤ ņøÉņ×ÉļĪ£ ļāēĻ░ü ņżæ ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ļÉĀ ņłś ņ׳ļŗż.
ņłśņåī ļåŹļÅäĻ░Ć ņłśņåī Ļ│ĀņÜ® ĒĢ£ļÅäļź╝ ļäśņ£╝ļ®┤ ņĘ©ņĢĮĒĢ£ ņłśņåīĒÖöļ¼╝ņØä ņäØņČ£ĒĢśņŚ¼ ĒīīĻ┤┤ņØĖņä▒ņØä ņĀĆĒĢśņŗ£Ēéżļ»ĆļĪ£ ņøÉņ×ÉļĪ£ Ļ░ĆļÅÖ ņżæņØś ņ┤Ø ņłśņåī ļåŹļÅäļŖö ļ¦żņÜ░ ņżæņÜöĒĢśļŗż [7]. ļśÉĒĢ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļé┤ņØś ņłśņåīļŖö ĻĘĀņŚ┤ ņäĀļŗ©ņŚÉņØś ņØæļĀź ņ¦æņżæ ļČĆņ£äņŚÉņä£ ņāüļīĆņĀüņ£╝ļĪ£ ņēĮĻ▓ī ņäØņČ£ĒĢśļ®░ ņłśņåīņ¦ĆņŚ░ ĒīīĻ┤┤ (delayed hydride cracking, DHC) ĻĖ░ĻĄ¼ņŚÉ ņØśĒĢ£ ĻĘĀņŚ┤ ņĀäĒīīļź╝ ņØ╝ņ£╝ĒéżĻĖ░ ļĢīļ¼ĖņØ┤ļŗż [8-11]. ņØ┤ļ¤░ ņØ┤ņ£ĀļĪ£ ņĢĢļĀźĻ┤ĆņŚÉņä£ ņłśņåī ļ░Å ņżæņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆļŖö ņĢĢļĀźĻ┤Ć Ļ▒┤ņĀäņä▒ņØä Ļ░Ćņן ņ£äĒśæĒĢśļŖö ņÜöņØĖ ņżæ ĒĢśļéśņØ┤ļŗż. ņØ┤ņŚÉ ļö░ļØ╝ Ļ░ĆļÅÖ ņĢĢļĀźĻ┤ĆņØś ņ┤Ø ņłśņåī ļåŹļÅäļŖö ņØ╝ņĀĢ ņŻ╝ĻĖ░ļź╝ ļö░ļØ╝ ņČöņĀü ļ░Å Ļ┤Ćļ”¼ļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż [12].
ņĢĢļĀźĻ┤ĆņØś roll joint ņŻ╝ņ£äņØś ĒŖ╣ņĀĢ ļČĆņ£äļŖö ņżæņłśņåīņØś ņ╣©Ēł¼Ļ░Ć ļ╣Āļź┤Ļ▓ī ņØ┤ļŻ©ņ¢┤ņ¦Ćļ»ĆļĪ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ņłśņåī ļåŹļÅäņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ņØ┤ ņ¢┤ļ¢╗Ļ▓ī ņäØņČ£ĒĢśļŖöņ¦Ćļź╝ ņØ┤ĒĢ┤ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ļŗż. ĒŖ╣Ē׳ ņĢĢļĀźĻ┤ĆņŚÉņä£ ņĄ£ļīĆ ņØæļĀźņØ┤ ņ×æņÜ®ĒĢśļŖö ļ░®Ē¢źņØĆ ĒÜĪ ļ░®Ē¢źņØ┤ļ»ĆļĪ£ ĒÜĪ ļ░®Ē¢źņŚÉ ņłśņ¦üĒĢ£ ņłśņåīĒÖöļ¼╝ņØĆ DHC ĻĖ░ĻĄ¼ņŚÉ ņØśĒĢ£ ņåÉņāüņØ┤ļéś ĒīīĻ┤┤ņØĖņä▒ņØś ņĀĆĒĢśņŚÉ Ēü░ ņśüĒ¢źņØä ļ»Ėņ╣£ļŗż [8-11].
Zr-2.5%Nb ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ▒░ļÅÖņØä ņØ┤ĒĢ┤ĒĢśļŖö Ļ▓āņØĆ ņżæņÜöĒĢśņ¦Ćļ¦ī [13], ņØ┤ņŚÉ ļīĆĒĢ£ ņĀĢļ¤ēņĀüņØĖ ņäØņČ£ Ļ▒░ļÅÖ ĒÅēĻ░Ć ņŚ░ĻĄ¼ļŖö Ļ▒░ņØś ņŚåņŚłļŗż. ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ļŖö ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ņłśņåī ļåŹļÅä ļ░Å ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäļź╝ ļ│ĆĒÖöņŗ£Ēé© ņŗ£ĒÄĖņØä ļ¦īļōżĻ│Ā Ļ┤æĒĢÖĒśäļ»ĖĻ▓Įņ£╝ļĪ£ ņłśņåīĒÖöļ¼╝ņØä Ļ┤Ćņ░░ĒĢ£ Ēøä MATLABņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢśņŚ¼ ņØ┤ļōż ļ│ĆņłśĻ░Ć ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ▒░ļÅÖņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä ņĄ£ņ┤łļĪ£ ņĪ░ņé¼ĒĢśņśĆļŗż. ņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļźĖ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ ļ│ĆĒÖöņÖĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ ņäØņČ£ ĒŖ╣ņä▒ņØ┤ ļŗ¼ļØ╝ņ¦ĆļŖö ņØ┤ņ£ĀņŚÉ ļīĆĒĢśņŚ¼ ļģ╝ņØśĒĢśņśĆļŗż.
2. ņŗż ĒŚś
ņŗżĒŚśņŚÉ ņé¼ņÜ®ĒĢ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļŖö Zr-2.5%Nb ĒĢ®ĻĖłņ£╝ļĪ£ ĒÖöĒĢÖ ņĪ░ņä▒ņØĆ Ēæ£ 1ņŚÉ ļ│┤ņśĆļŗż. ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļŖö 30 ├Ś 100 mm ņĀĢļÅäļĪ£ ņĀłļŗ©ĒĢ£ Ēøä Ēæ£ļ®┤ņØä Ļ┤æĒāØņØ┤ ļéśļÅäļĪØ ņŚ░ļ¦łĒĢśņśĆļŗż. 1 Mol ĒÖ®ņé░ ņÜ®ņĢĪņØä ņé¼ņÜ®ĒĢśņŚ¼ 85+/-5 ┬░CņŚÉņä£ 100 mA/cm2 ņØś ņĀäļźś ļ░ĆļÅäļĪ£ 24-40ņŗ£Ļ░ä ņĀäĒĢ┤ ļ░®ļ▓Ģņ£╝ļĪ£ ņ×¼ļŻī Ēæ£ļ®┤ņŚÉ ņłśņåīĒÖöļ¼╝ņØä ĒśĢņä▒ņŗ£ņ╝░ļŗż [6]. ņØ┤ ņŗ£ĒÄĖļōżņØĆ PyrexņÖĆ quartzļź╝ ņé¼ņÜ®ĒĢśņŚ¼ vacuum sealing Ēøä 300-550 ┬░CņØś ņĀäĻĖ░ļĪ£ņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņśĆļŗż. ĻĘĀņ¦łĒÖö ņ▓śļ”¼ļŖö 350 ┬░C ņØ┤ĒĢśņŚÉņä£ 500ņŗ£Ļ░ä, 400 ┬░C ņØ┤ņāüņŚÉņä£ 240ņŗ£Ļ░ä ņ£Āņ¦ĆĒĢśņśĆļŗż. ņØ┤ ņ£Āņ¦Ć ņŗ£Ļ░äņØĆ ņłśņåīĻ░Ć ĻĘĀņ¦łĒÖöļÉśļŖöļŹ░ ĒĢäņÜöĒĢ£ ņŗ£Ļ░äņØś 20ļ░░ ņØ┤ņāüņØ┤ļŗż. Vacuum sealing tubeļŖö ĻĘĀņ¦łĒÖö ņŚ┤ņ▓śļ”¼ Ēøä Ļ│ĄĻĖ░ ņżæņŚÉņä£ ļāēĻ░üĒĢśņśĆļŗż. Ļ│ĄĻĖ░ ņżæņŚÉņä£ ļāēĻ░üĒĢśņśĆņ¦Ćļ¦ī ļāēĻ░ü ņĪ░Ļ▒┤ņØĆ vacuum sealing tubeņØś ņŚ┤ņĀäļŗ¼ ĒŖ╣ņä▒ņāü ļāēĻ░ü Ļ│╝ņĀĢņØĆ ņä£ņä£Ē׳ ļāēĻ░üļÉ£ Ļ▓āĻ│╝ ņ£Āņé¼ĒĢśļŗż. ņØ┤ ņĪ░Ļ▒┤ļōżņØĆ Ēæ£ 2ņŚÉ ņÜöņĢĮĒĢśņŚ¼ ļéśĒāĆļé┤ņŚłļŗż.
ņłśņåīĒÖöļ¼╝ņØĆ ņŚ░ļ¦łņÖĆ HF + HNO3+ H2O ņÜ®ņĢĪņ£╝ļĪ£ etchingĒĢśņŚ¼ Ļ┤æĒĢÖ Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ņłśņåīĒÖöļ¼╝ņØś Ļ┤Ćņ░░ņØĆ 200ļ░░ļĪ£ ņŗżņŗ£ĒĢśņśĆņ£╝ļ®░, Ļ░ü ņŗ£ĒŚśĒÄĖņŚÉ ļīĆĒĢśņŚ¼ Ļ░üĻ░ü ļŗżļźĖ ļČĆņ£äņŚÉņä£ 20ņןņØś Ļ┤æĒĢÖ ņé¼ņ¦äņØä ņ┤¼ņśüĒĢśņśĆļŗż. ņØ┤ļź╝ MATLAB imageņ£╝ļĪ£ ņĀĢļ¤ēņĀü ņ▓śļ”¼ĒĢśņŚ¼ ņłśņåīĒÖöļ¼╝ņØś ņłś, ĻĖĖņØ┤, ļæÉĻ╗ś, ļ®┤ņĀü ļ╣äņ£© (area fraction) ļō▒ņØä ņĖĪņĀĢĒĢśņśĆļŗż.
ņłśņåī ņןņ×ģ ļ░Å ĻĘĀņ¦łĒÖö ņ▓śļ”¼ Ēøä ļ»ĖņäĖņĪ░ņ¦üņØś ļ│ĆĒÖöļŖö Ēł¼Ļ│╝ņĀäņ×ÉĒśäļ»ĖĻ▓Į(TEM)ņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ņĀäĒĢ┤ ņŚ░ļ¦ł ņÜ®ņĢĪņØĆ 10% Perchloric acid +Methanol ņÜ®ņĢĪņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░ ŌĆō35 ┬▒ 5 ┬░CņŚÉņä£ ņĀäĒĢ┤ ņŚ░ļ¦łĒĢśņśĆļŗż. ļ»ĖņäĖņĪ░ņ¦ü Ļ┤Ćņ░░ņØĆ JEOL JEM2100F TEMņØä ņé¼ņÜ®ĒĢśņśĆļŗż.
ĻĘĀņ¦łĒÖö ņ▓śļ”¼ļÉ£ ņŗ£ĒÄĖņØś ņłśņåī ļåŹļÅäļŖö LECOņé¼ņØś gas ļČäņäØĻĖ░ļź╝ ņé¼ņÜ®ĒĢśņśĆļŗż. ņØ┤ ļ░®ļ▓ĢņØĆ Ļ│Āņś© extraction ļ░®ļ▓Ģņ£╝ļĪ£ ņłśņåīļź╝ ņČöņČ£ĒĢśĻ│Ā ņłśņåīĻ░Ć ĒżĒĢ©ļÉ£ carrier gasņØś ņŚ┤ņĀäļÅäļÅäļź╝ ņĖĪņĀĢĒĢśņŚ¼ ņłśņåī ļåŹļÅäļź╝ ņĖĪņĀĢĒĢśļŖö ļ░®ļ▓ĢņØ┤ļŗż. ļČäņäØ ņŗĀļó░ļÅäļź╝ ļåÆņØ┤ĻĖ░ ņ£äĒĢśņŚ¼ ņŗ£ĒŚś ņןļ╣äņØś ļ│┤ņĀĢņØĆ ļČäņäØ ņŗ£ĒÄĖņŚÉņä£ ņśłņāüļÉśļŖö ņłśņåī ļåŹļÅäņÖĆ ņ£Āņé¼ĒĢ£ Ēæ£ņżĆ ņŗ£ļŻīļź╝ ļČäņäØĒĢśļŖö ļ░®ļ▓Ģņ£╝ļĪ£ ņØ┤ļŻ©ņ¢┤ņ¦äļŗż. ņłśņåī ļČäņäØņØĆ 300 mg ņĀĢļÅäņØś ņŗ£ĒÄĖņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░ ļČäņäØļÉ£ ņłśņåī ļåŹļÅäļŖö 3Ļ░£ņØś ļČäņäØ Ļ▓░Ļ│╝ļź╝ ĒÅēĻĘĀĒĢ£ Ļ▓āņØ┤ļŗż.
ņłśņåī ļåŹļÅä ļČäņäØ Ļ▓░Ļ│╝ņØś Ēæ£ņżĆ ĒÄĖņ░©ļŖö ļīĆļץ ┬▒2 ppmņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż. ņłśņåī ļåŹļÅäļŖö as-received ņŗ£ĒÄĖņŚÉņä£ 14 ppmņØ┤Ļ│Ā, ņłśņåīļź╝ ņןņ×ģĒĢśĻ│Ā ĻĘĀņ¦łĒÖö ņŗ£Ēé© ņŗ£ĒÄĖņØś ļåŹļÅäļŖö 28-144 ppm ļ▓öņ£äļĪ£ ļéśĒāĆļé¼ļŗż. ņØ┤ ņŗ£ĒÄĖļōżņØĆ ņłśņåī ļåŹļÅäņÖĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļźĖ ņäØņČ£ Ēī©Ēä┤ņØä ļČäņäØĒĢśļŖöļŹ░ ņ£ĀņÜ®ĒĢśņśĆļŗż.
3. Ļ▓░ Ļ│╝
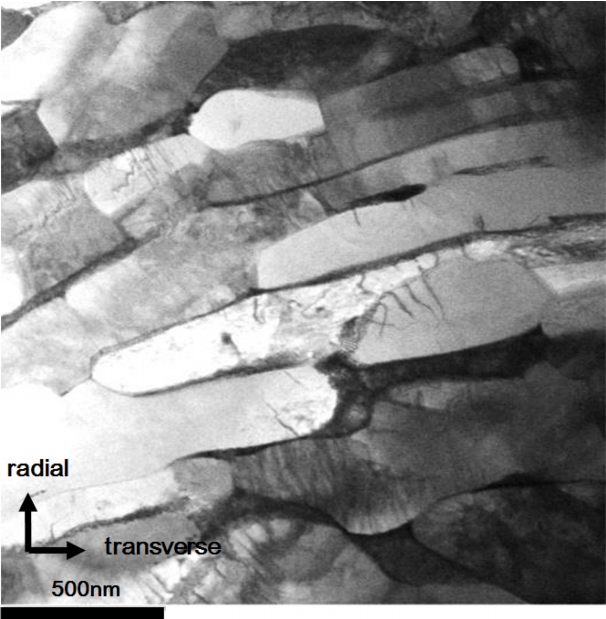
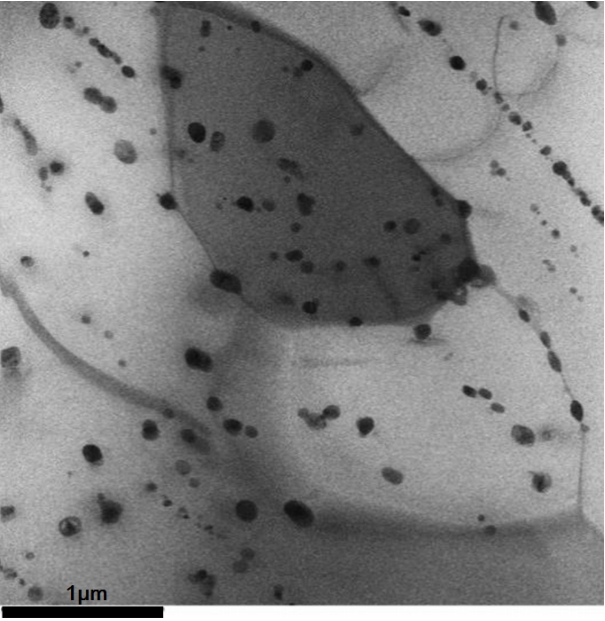
ņŗżĒŚśņŚÉ ņé¼ņÜ®ĒĢ£ as-received Zr-2.5%Nb ĒĢ®ĻĖł ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś TEM ļ»ĖņäĖņĪ░ņ¦üņØĆ ĻĘĖļ”╝ 1ņŚÉ ļ│┤ņśĆļŗż. ļ»ĖņäĖņĪ░ņ¦üņØĆ ņĢĢļĀźĻ┤ĆņØś ĻĖĖņØ┤ ļ░®Ē¢źņŚÉ ņłśņ¦üĒĢ£ ļ®┤ņŚÉņä£ Ļ┤Ćņ░░ĒĢ£ Ļ▓āņØ┤ļŗż. Asreceived Zr-2.5%Nb ĒĢ®ĻĖłņØś ļ»ĖņäĖņĪ░ņ¦üņØĆ ╬▒-Zr Ļ▓░ņĀĢļ”ĮņØ┤ ņĢĢļĀźĻ┤ĆņØś ļæÉĻ╗ś ļ░®Ē¢źņ£╝ļĪ£ ļé®ņ×æĒĢśĻ▓ī ļ│┤ņØ┤Ļ│Ā ĻĘĖ Ļ│äļ®┤ņŚÉ ╬▓-Zrņ£╝ļĪ£ ļŹ«ņŚ¼ ņ׳ļŗż.
ĻĘĖļ”╝ 2 (a)ļŖö 28 ppm (300 ┬░C ĻĘĀņ¦łĒÖö), (b)ļŖö 64 ppm (400 ┬░C ĻĘĀņ¦łĒÖö), (c)ļŖö 144 ppm (500 ┬░C ĻĘĀņ¦łĒÖö)ņØś ņłśņåīļź╝ ĒĢ©ņ£ĀĒĢ£ ņŗ£ĒÄĖņØś ņłśņåīĒÖöļ¼╝ņØś ĒśĢņāüņØä ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ņØĆ ņĢĢļĀźĻ┤ĆņØś ĒÜĪ ļ░®Ē¢źņ£╝ļĪ£ ĻĖĖĻ▓ī ņäØņČ£ļÉ£ļŗż. ņØ┤Ļ▓āņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ĻĖĖņØ┤ ļ░Å ĒÜĪ ļ░®Ē¢źņØä ļö░ļØ╝ ĒīÉņāüņ£╝ļĪ£ ņäØņČ£ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ļŗ©ļ®┤ņ£╝ļĪ£ļŖö ĻĖĖĻ▓ī ļŖśņ¢┤ļé£ ņäĀņ£╝ļĪ£ ļ│┤ņØĖļŗż. ņłśņåī ļåŹļÅä ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ļŖö ņ”ØĻ░ĆĒĢśĻ│Ā ņäØņČ£ļ¼╝ ņé¼ņØ┤ņØś Ļ▒░ļ”¼Ļ░Ć ņ¦¦ņĢäņ¦äļŗż.
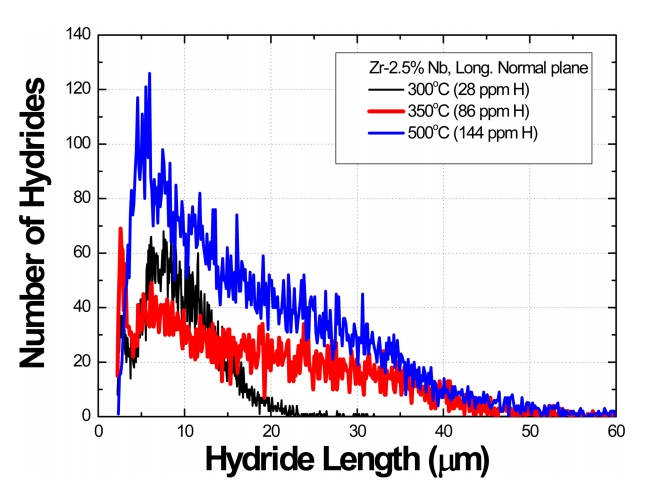
ĻĘĖļ”╝ 3ņØĆ ņłśņåīĒÖöļ¼╝ ĻĖĖņØ┤ņŚÉ ļö░ļźĖ ļ╣łļÅäļź╝ ĻĘĖļלĒöäļĪ£ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. 300 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ 28 ppmņØś ņłśņåīļź╝ ĒĢ©ņ£ĀĒĢ£ ņŗ£ĒÄĖņØĆ ļīĆļČĆļČäņØś ņłśņåīĒÖöļ¼╝ņØĆ 20 ╬╝m ņØ┤ĒĢśņØ┤Ļ│Ā ņĄ£ļīĆ ļ╣łļÅäļŖö 8-10 ╬╝m ņĀĢļÅäņŚÉņä£ ļéśĒāĆļé£ļŗż. 350 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ ņłśņåī ļåŹļÅäĻ░Ć 86 ppmņØĖ Ļ▓ĮņÜ░ļŖö ņĄ£ļīĆ 40 ╬╝m ņĀĢļÅäņØś ņłśņåīĒÖöļ¼╝ņØ┤ ĒśĢņä▒ļÉśĻ│Ā ĻĖĖņØ┤Ļ░Ć 5-15 ╬╝m ņĀĢļÅäņØĖ ņłśņåīĒÖöļ¼╝ņØ┤ 30Ļ░£ ņĀĢļÅäņØś ļ╣łļÅäļĪ£ ņäØņČ£ĒĢ£ļŗż. 500 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ 144 ppmņØś ņłśņåīļź╝ ĒĢ©ņ£ĀĒĢ£ ņŗ£ĒÄĖņŚÉ ļīĆĒĢ£ Ļ▓āņ£╝ļĪ£ 5-15 ╬╝m ņĀĢļÅäņØś ņłśņåīĒÖöļ¼╝ņØś ļ╣łļÅäĻ░Ć 80Ļ░£ ņĀĢļÅäļĪ£ ļéśĒāĆļéśļ®░ ņĄ£ļīĆ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ļŖö 50 ╬╝m ņĀĢļÅäņØ┤ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņĀ£ņ×æĒĢ£ 9Ļ░£ņØś ņŗ£ĒÄĖņŚÉ ļīĆĒĢśņŚ¼ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤, ļ╣äņ£© (=ĻĖĖņØ┤/ļæÉĻ╗ś), ļ®┤ņĀü ļČäņ£© ļō▒ņØś ĒŖ╣ņä▒ ņ×ÉļŻīļŖö Ēæ£ 3ņŚÉ ņÜöņĢĮĒĢśņśĆļŗż. Ēæ£ 3ņØĆ Zr-2.5%Nb ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ņłśņåī ļåŹļÅä ļ░Å ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļźĖ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ĒŖ╣ņä▒ņØä ņĄ£ņ┤łļĪ£ ņĀĢļ¤ē ļČäņäØĒĢ£ Ļ▓āņØ┤ļŗż.
Ēæ£ 4ļŖö 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ņŗ£ĒÄĖņŚÉņä£ ņłśņåīĒÖöļ¼╝ ņäØņČ£ ĒŖ╣ņä▒ņØä ņĀĢļ”¼ĒĢśņŚ¼ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓āļ¦īņØä ļö░ļĪ£ ļ╣äĻĄÉĒĢ£ ņØ┤ņ£ĀļŖö 400 ┬░C ņØ┤ņāüņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ ╬▓-Zr ņāüņØś ļČäĒĢ┤Ļ░Ć ņØ╝ņ¢┤ļéśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ņØ┤ Ēæ£ņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØś ļČäņ£©ņØĆ Ļ┤æĒĢÖĒśäļ»ĖĻ▓Į ņé¼ņ¦äņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØ┤ ņ░©ņ¦ĆĒĢśļŖö ļ®┤ņĀüņØś ļ╣äņ£©ņØ┤Ļ│Ā, ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö Ļ┤æĒĢÖĒśäļ»ĖĻ▓Į ņé¼ņ¦ä 1ņןļŗ╣ ņäØņČ£ļÉśļŖö ņłśņåīĒÖöļ¼╝ņØś ņłśņØ┤ļŗż.
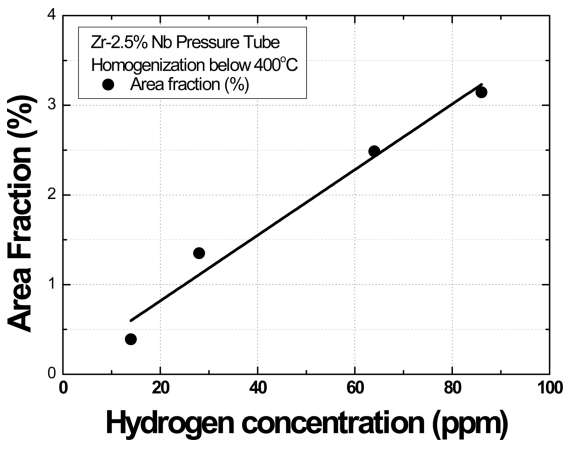
ĻĘĖļ”╝ 4ļŖö Ēæ£ 4ņŚÉ ļ│┤ņØĖ ņłśņåīĒÖöļ¼╝ ļČäņ£©ņØä ņłśņåī ļåŹļÅäņŚÉ ļö░ļØ╝ ļÅäņŗ£ĒĢ£ Ļ▓āņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ņØś ļČäņ£©ņØĆ ņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ Ļ▒░ņØś ņ¦üņäĀņĀüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśĻ│Ā, ņłśņåīĒÖöļ¼╝ņØś ļ®┤ņĀüņØĆ ņłśņåī ļåŹļÅäņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ņ”ØĻ░ĆĒĢ£ļŗżļŖö Ļ▓āņØä ņל ļ│┤ņŚ¼ ņżĆļŗż. ņØ┤ Ļ▓░Ļ│╝ļŖö ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØś ņĀĢļ¤ēņĀüņØĖ ĒÅēĻ░Ćļź╝ ņ£äĒĢśņŚ¼ ņé¼ņÜ®ĒĢ£ MATLAB image ņĀüņÜ®ņØ┤ ļ¦żņÜ░ ĒĢ®ļŗ╣ĒĢśļŗżļŖö Ļ▓āņØä ļéśĒāĆļé┤ļŖö Ļ▓āņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ Ļ┤Ćņ░░ ņé¼ņ¦äņØä MATLAB imageņŚÉ ņĀüņÜ®ĒĢśļ®┤ ņ×¼ļŻīņØś ņłśņåī ļåŹļÅäļź╝ Ļ░£ļץņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŗżļŖö ņØśļ»ĖņØ┤ĻĖ░ļÅä ĒĢśļŗż.
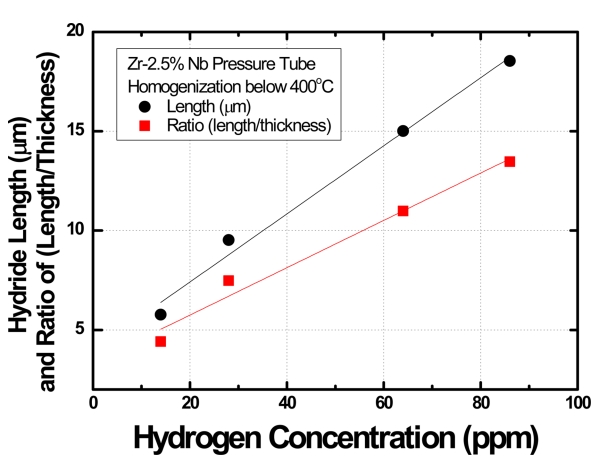
ĻĘĖļ”╝ 5ļŖö Ēæ£ 4ņŚÉ ļéśĒāĆļéĖ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ņÖĆ ņłśņåīĒÖöļ¼╝ņØś ļ╣äņ£©(ĻĖĖņØ┤/ļæÉĻ╗ś)ņØä ņłśņåī ļåŹļÅäņŚÉ ļö░ļØ╝ ļÅäņŗ£ĒĢ£ Ļ▓āņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ņÖĆ ļ╣äņ£©ņØĆ ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ņ¦üņäĀņĀüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢ£ļŗż.
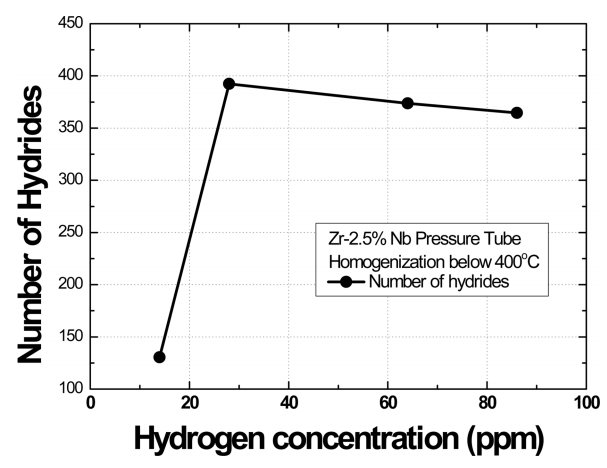
ĻĘĖļ”╝ 6ņØĆ Ēæ£ 4ņŚÉ ļéśĒāĆļéĖ ņłśņåīĒÖöļ¼╝ņØś ņłśļź╝ ņłśņåī ļåŹļÅäņŚÉ ļö░ļØ╝ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ņłśņåī ļåŹļÅäĻ░Ć ņĢĮ 30 ppm ņĀĢļÅäĻ╣īņ¦ĆļŖö ĻĖēĻ▓®Ē׳ ņ”ØĻ░ĆĒĢśņŚ¼ 400Ļ░£ ņĀĢļÅäņŚÉ ņØ┤ļź┤Ļ│Ā ņłśņåī ļåŹļÅäĻ░Ć ņ”ØĻ░ĆĒĢśņŚ¼ļÅä ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö ņ”ØĻ░ĆĒĢśņ¦Ć ņĢŖĻ│Ā 400Ļ░£ ļé┤ņÖĖņØś ņØ╝ņĀĢĒĢ£ Ļ░ÆņØä ļéśĒāĆļéĖļŗż. ņØ┤Ļ▓āņØĆ ņłśņåī ļåŹļÅäĻ░Ć ņ”ØĻ░ĆĒĢĀ ļĢī ņ¦¦ņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņä£ļĪ£ ņ¢┤ņØ┤ņ¦ĆļŖö ĒśĢĒā£ļĪ£ ņäØņČ£ĒĢśĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
Table┬Ā5.
Summary of hydride precipitation parameters with 81-86 ppm homogenized at 350-475 ┬░C in Zr-2.5%Nb pressure tube material.
ĻĘĖļ”╝ 7 (a)ļŖö 86 ppm (350 ┬░C ĻĘĀņ¦łĒÖö), (b)ļŖö 81 ppm (400 ┬░C ĻĘĀņ¦łĒÖö), (c)ļŖö 82 ppm (475 ┬░C ĻĘĀņ¦łĒÖö)ņØś ņłśņåīļź╝ ĒĢ©ņ£ĀĒĢ£ ņŗ£ĒÄĖņØś ņłśņåīĒÖöļ¼╝ņØś ĒśĢņāüņØä ļ╣äĻĄÉĒĢśņŚ¼ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ņØ┤ļōż ņŗ£ĒÄĖņØś ņłśņåī ļåŹļÅäļŖö ņä£ļĪ£ ļ╣äņŖĘĒĢśņ¦Ćļ¦ī ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäļŖö Ļ░üĻ░ü ļŗżļź┤ļŗż. ĻĘĖļ”╝ 7ņØĆ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ▒░ļÅÖņØ┤ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļØ╝ ļŗ¼ļØ╝ņ¦äļŗżļŖö Ļ▓āņØä ļ│┤ņØĖļŗż. ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ļ░®Ē¢źņØ┤ 400 ┬░C ņØ┤ĒĢśņŚÉņä£ļŖö ĒÜĪ ļ░®Ē¢źņ£╝ļĪ£ ņäØņČ£ĒĢśļŖö ļ░śļ®┤ 475 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓āņØĆ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ļ░®Ē¢źņØ┤ ļ¼┤ņ×æņ£äĒĢśĻ▓ī ļ░öļĆÉļŗż. ļśÉĒĢ£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäĻ░Ć ņ”ØĻ░ĆĒĢśļ®┤ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ļŖö ņ¦¦ņĢäņ¦ĆĻ│Ā ņĀÉņ░© ļæÉĻ║╝ņøīņ¦ĆļŖö Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż.
ĻĘĖļ”╝ 7 (b) ļ░Å (c)ņŚÉņä£ ņĢī ņłś ņ׳ļŖö ļ░öņÖĆ Ļ░ÖņØ┤ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäĻ░Ć 400 ┬░C ņØ┤ņāüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśļ®┤ ╬▒-ZrĻ│╝ ╬▓-ZrņØś ļČäĒĢ┤Ļ░Ć ņØ╝ņ¢┤ļéś 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ļÉ£ Ļ▓āĻ│╝ ļŗżļźĖ ņäØņČ£ Ļ▒░ļÅÖņØä ļ│┤ņØ┤ļŖö Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ņØ┤Ļ▓āņØĆ ĻĘĖļ”╝ 4ņŚÉņä£ ņäżļ¬ģĒĢ£ ļ░öņÖĆ Ļ░ÖņØ┤ ņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ņØ┤ ņä▒ņןĒĢĀ ļĢī ņ×æņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņØ┤ņ¢┤ņ¦Ćņ¦Ć ņĢŖĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ļ│┤ņØĖļŗż. ņØ┤Ļ▓āņØĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ņØś ņłśĻ░Ć ņ”ØĻ░ĆĒĢśļŖö Ļ▓āņ£╝ļĪ£ļČĆĒä░ ĒÖĢņØĖĒĢĀ ņłś ņ׳ļŗż.
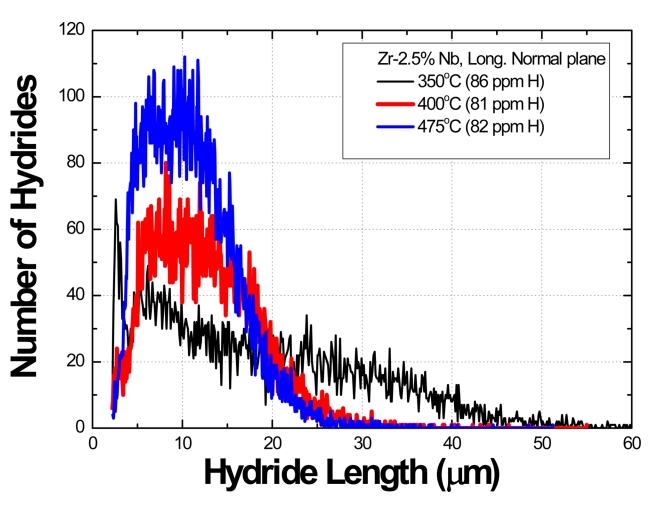
ĻĘĖļ”╝ 8ņØĆ ĻĘĖļ”╝ 5ņŚÉ ļéśĒāĆļéĖ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ņÖĆ ĻĘĖņŚÉ ļīĆĒĢ£ ļ╣łļÅäļź╝ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. 350 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ ņłśņåī ļåŹļÅäĻ░Ć 86 ppmņØĖ Ļ▓ĮņÜ░ļŖö 3 ╬╝m ņĀĢļÅäļĪ£ ņ¦¦ņØĆ Ļ▓āņ£╝ļĪ£ļČĆĒä░ 50 ╬╝m ņĀĢļÅäĻ╣īņ¦Ć ņäØņČ£ ļ╣łļÅäĻ░Ć ņĀÉņ¦äņĀüņ£╝ļĪ£ Ļ░ÉņåīĒĢ£ļŗż. 400 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ ņłśņåī ļåŹļÅäĻ░Ć 81 ppmņØĖ Ļ▓ĮņÜ░ļŖö 5-15 ╬╝m ņĀĢļÅäņØś ņłśņåīĒÖöļ¼╝ņØ┤ 60Ļ░£ ņĀĢļÅäļĪ£ ĒśĢņä▒ļÉśĻ│Ā, ņĄ£ļīĆ 30 ╬╝m ņĀĢļÅäņØś Ēü¼ĻĖ░Ļ╣īņ¦Ć ĒśĢņä▒ļÉ£ļŗż. 475 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ 82 ppmņØĖ Ļ▓ĮņÜ░ļŖö ņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ 5-15 ╬╝m ņĀĢļÅäņØś ņłśņåīĒÖöļ¼╝ņØ┤ 100Ļ░£ ņĀĢļÅäņØś ļ╣łļÅäļĪ£ ņäØņČ£ļÉ£ļŗż.
ĻĘĖļ”╝ 9ļŖö ĻĘĖļ”╝ 7 ļ░Å 8ņŚÉ ļ│┤ņØĖ ņŗ£ĒÄĖņØś ņłśņåīĒÖöļ¼╝ņØś ņłś, ļæÉĻ╗ś, ļ╣äņ£©(ĻĖĖņØ┤/ļæÉĻ╗ś)ņØä ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļØ╝ ļÅäņŗ£ĒĢ£ Ļ▓āņØ┤ļŗż. ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäĻ░Ć 350ņŚÉņä£ 400, 475 ┬░CļĪ£ ņ”ØĻ░ĆĒĢśļ®┤ ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö 160%, 230%ļĪ£ ņ”ØĻ░ĆĒĢ£ļŗż. ņØ┤ ņØ┤ņ£ĀļŖö ņś©ļÅäņØś ņ”ØĻ░ĆņŚÉ ņØśĒĢ┤ ņłśņåīĒÖöļ¼╝ņØś ņłśĻ░Ć ņ”ØĻ░ĆĒĢ£ ĒÜ©Ļ│╝ņÖĆ ļæÉĻ╗śņØś ņ”ØĻ░ĆņŚÉ ņØśĒĢ£ ĒÜ©Ļ│╝Ļ░Ć ĒżĒĢ©ļÉśņŚłĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ĻĘĖļ”╝ņŚÉļŖö ļéśĒāĆļé┤ņ¦Ć ņĢŖņĢśņ¦Ćļ¦ī, ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäĻ░Ć 350ņŚÉņä£ 400, 475 ┬░CļĪ£ ļåÆņĢäņ¦Ćļ®┤ ĻĖĖņØ┤ 30-50 ╬╝m ļ▓öņ£äņØś ņłśņåīĒÖöļ¼╝ņØś ļ╣łļÅäļŖö Ļ░ÉņåīĒĢ£ļŗż. 400 ŌäāļĪ£ ņ”ØĻ░ĆĒĢśļ®┤ ĻĖĖņØ┤ 5-15 ╬╝m ņĀĢļÅäņØś ņłśņåīĒÖöļ¼╝ ļ╣łļÅäĻ░Ć ņ”ØĻ░ĆĒĢ£ļŗż. 475 ┬░CļĪ£ ņ”ØĻ░ĆĒĢśļ®┤ 5-15 ╬╝m ņĀĢļÅäņØś ļ╣łļÅäĻ░Ć ĒśäņĀĆĒ׳ ņ”ØĻ░ĆĒĢ£ļŗż. ņ”ē, ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ņØĆ ņ¦¦ņĢäņ¦ĆĻ│Ā ņł½ņ×ÉļŖö ļ¦ÄņĢäņ¦ĆļŖö Ļ▓āņØä ņĢī ņłś ņ׳ļŗż.
ĻĘĖļ”╝ 10 (a)ļŖö ņłśņåī ļåŹļÅäĻ░Ć 64 ppm ņØĖ Ļ▓ĮņÜ░ņÖĆ ĻĘĖļ”╝ 10 (b)ļŖö 54 ppmņØĖ Ļ▓ĮņÜ░ļź╝ ļ╣äĻĄÉĒĢśņŚ¼ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ĻĘĖļ”╝ 10 (a)ļŖö 400 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓āņ£╝ļĪ£ ĒÜĪ ļ░®Ē¢źņŚÉ ĒÅēĒ¢ēĒĢśĻ▓ī ņäØņČ£ļÉ£ ņłśņåīĒÖöļ¼╝ņØ┤ ļīĆļČĆļČäņØ┤ļŗż. ĻĘĖņŚÉ ļ░śĒĢ┤, 550 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ĻĘĖļ”╝ 10 (b)ļŖö ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ļ░®Ē¢źņØ┤ Ļ▒░ņØś randomĒĢśļŗż. ņØ┤ņÖĆ Ļ░ÖņØ┤ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ▒░ļÅÖņØ┤ ļŗ¼ļØ╝ņ¦ĆļŖö Ļ▓āņØĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ Ļ│╝ņĀĢņŚÉ ļéśĒāĆļéśļŖö ļ»ĖņäĖņĪ░ņ¦üņØś ļ│ĆĒÖö ļĢīļ¼Ėņ£╝ļĪ£ ļ│┤ņØĖļŗż. ņØ┤ļ¤░ Ļ▒░ļÅÖņØĆ ĻĘĖļ”╝ 7 (b) ļ░Å (c)ņŚÉņä£ ļéśĒāĆļé£ Ļ▒░ļÅÖĻ│╝ ņ£Āņé¼ĒĢśļŗż.
ĻĘĖļ”╝ 11ņØĆ ļ│Ė ņŚ░ĻĄ¼ņŚÉ ņé¼ņÜ®ļÉ£ ņŗ£ĒŚśĒÄĖņŚÉņä£ 14-144 ppmņØś ņłśņåī ļåŹļÅäņŚÉ ļö░ļźĖ ņłśņåīĒÖöļ¼╝ņØś ļČäņ£©ņØä ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ņØś ļČäņ£©ņØĆ ņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ Ļ▒░ņØś ņ¦üņäĀņĀüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢ£ļŗż. ņØ┤ Ļ▓░Ļ│╝ļŖö 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓░Ļ│╝ļź╝ ļéśĒāĆļéĖ ĻĘĖļ”╝ 4ņÖĆ Ļ░ÖņØĆ Ļ▓ĮĒ¢źņØä ļ│┤ņØĖļŗż.
ĻĘĖļ”╝ 12ņØĆ 400 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ļÅÖņĢł ņłśņåī ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś ļ»ĖņäĖņĪ░ņ¦üņØä ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ĻĘĖļ”╝ 1Ļ│╝ ļ╣äĻĄÉĒĢśļ®┤ 400 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ ņŚ░ņåŹņĀüņØĖ ņĪ░ņ¦üņØś ╬▓-ZrņØ┤ ļČäĒĢ┤ļÉśņ¢┤ ļŗ©ņåŹņĀüņØĖ ĒśĢĒā£ļĪ£ ļ░öļĆīļŖö Ļ▓āņØä ņĢī ņłś ņ׳ļŗż. ņ”ē, ╬▓-ZrņØĆ ņ┤łĻĖ░ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ╬▒-Zr Ļ│äļ®┤ņŚÉ ņŚ░ņåŹņĀüņØĖ ĒĢäļ”ä ĒśĢĒā£ņŚÉ Ļ░ĆĻ╣īņÜ┤ ņāüĒā£ļĪ£ ņĪ┤ņ×¼ĒĢśņśĆņ£╝ļéś ļČäĒĢ┤ļÉśĻĖ░ ņŗ£ņ×æĒĢśņŚ¼ ļČłņŚ░ņåŹņĀüņØĖ ĒśĢĒā£ļĪ£ ļ░öļĆÉļŗż.
ĻĘĖļ”╝ 13ņØĆ 475 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ļÅÖņĢł ņłśņåī ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś ļ»ĖņäĖņĪ░ņ¦üņØä ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ļ»ĖņäĖņĪ░ņ¦üņØĆ ╬▓-ZrņØ┤ ļČäĒĢ┤ļÉśĻ│Ā ╬▓-NbņØś ĒśĢĒā£Ļ░Ć ļ│ĆĒÖöĒ¢łņØä ļ┐Éļ¦ī ņĢäļŗłļØ╝ ╬▒-ZrņØś ņ×¼Ļ▓░ņĀĢņØä ņØ╝ņ£╝ņ╝£ ņ┤łĻĖ░ ╬▒-Zr Ļ▓░ņĀĢļ”ĮņØĆ ņé¼ļØ╝ņ¦äļŗż. ╬▓ ņāüņØĆ 400 ┬░C ņŚÉņä£ ņŚ┤ņ▓śļ”¼ĒĢ£ ņŗ£ĒÄĖļ│┤ļŗż ļŹö ļČäĒĢ┤ļÉśņ¢┤ ņĢĮĻ░ä ĻĖĖĻ▓ī ļŖśņ¢┤ļé£ ĻĄ¼ņāüņ£╝ļĪ£ ļ│┤ņØĖļŗż.
ĻĘĖļ”╝ 14ļŖö 550 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ļÅÖņĢł ņłśņåī ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś ļ»ĖņäĖņĪ░ņ¦üņØä ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. ╬▒-ZrņØĆ ņłś ╬╝mļĪ£ ņä▒ņןĒĢśņŚ¼ Ļ▓░ņĀĢļ”ĮņØś ļ¬©ņ¢æņØ┤ ļō▒ļ░®ņ£╝ļĪ£ ļ░öļĆīņŚłļŗż. ņĢäņÜĖļ¤¼ ╬▓ ņāüņØĆ 100 nm ņĀĢļÅäļĪ£ ņä▒ņןĒĢśņŚ¼ ĻĄ¼ņāüĒÖö ļÉśņŚłņ£╝ļ®░ ņ┤łĻĖ░ ╬▒-ZrņØä ļæśļ¤¼ņŗĖĻ│Ā ņ׳ļŹś ņ£äņ╣śņŚÉņä£ ļČäĒĢ┤ļÉśņ¢┤ ļé©ņĢä ņ׳Ļ▒░ļéś ņä▒ņןĒĢ£ Ļ▓░ņĀĢ ņé¼ņØ┤ņŚÉ ļé©ņĢä ņ׳ļŗż.
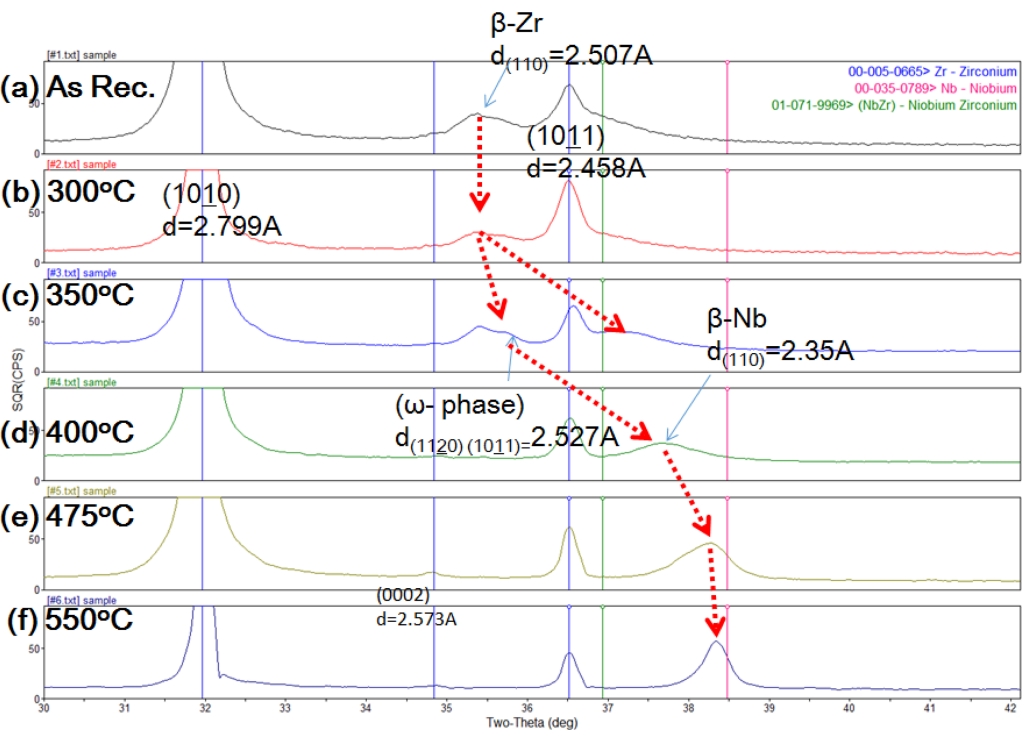
ĻĘĖļ”╝ 15ļŖö XRD ļČäņäØņŚÉ ņØśĒĢśņŚ¼ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ as-received ņāüĒā£ņŚÉņä£ ņĪ┤ņ×¼ĒĢśļŖö ╬▓-ZrņØś ļČäĒĢ┤ Ļ│╝ņĀĢņØä ļ╣äĻĄÉĒĢśņŚ¼ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż. 350 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ ╬▓-Zr ņāüņØś ņØ╝ļČĆĻ░Ć ļČäĒĢ┤ļÉśņ¢┤ Žē(omega) ņāüņØ┤ ļÉ£ļŗż. 400 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ ╬▓-Zr Ļ│╝ Žē ņāüņØĆ ņÖäņĀäĒ׳ ņé¼ļØ╝ņĀĖ ╬▓-NbņØ┤ ĒśĢņä▒ļÉśĻĖ░ ņŗ£ņ×æĒĢśņ¦Ćļ¦ī CuK╬▒ X-rayļĪ£ 2╬Ė 38.5┬░ ļČĆĻĘ╝ņŚÉ Ēæ£ņŗ£ļÉ£ ╬▓-Nb ņāüĻ│╝ļŖö ņĢĮĻ░ä ļŗżļź┤ļŗż. 475 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ Ļ▓®ņ×Éļ®┤ Ļ▒░ļ”¼Ļ░Ć ╬▓-NbņŚÉ ļŹöņÜ▒ ļŹö Ļ░ĆĻ╣īņøīņ¦ĆĻ│Ā, 550 ┬░CņŚÉņä£ ╬▓-Nb ņāüņŚÉ Ļ░ĆĻ╣īņøīņ¦äļŗż. ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäĻ░Ć 550 ┬░CļĪ£ ļåÆņĢäņ¦Ćļ®┤ ╬▓-NbĻ░Ć ĒśĢņä▒ļÉĀ ļ┐Éļ¦ī ņĢäļŗłļØ╝ ĻĘĖļ”╝ 14ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ ╬▒-Zr ņāüļÅä ņ╗żņ¦äļŗż.
4. ļģ╝ ņØś
Zr-2.5%Nb ĒĢ®ĻĖł ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ▒░ļÅÖņØä ņŚ░ĻĄ¼ĒĢśļŖö Ļ▓āņØĆ ņŗżņĀ£ Ļ░ĆļÅÖ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ▒░ļÅÖņØä ļ¬©ņé¼ĒĢśĻĖ░ ņ£äĒĢ£ Ļ▓āņØ┤ļŗż. ņŗżņĀ£ ņżæņłśļĪ£ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļŖö ņøÉņ×ÉļĪ£ Ļ░ĆļÅÖ ņĪ░Ļ▒┤ņØĖ 260-310 ┬░CņŚÉņä£ Ēæ£ļ®┤ņ£╝ļĪ£ļČĆĒä░ ņłśņåīļź╝ ĒØĪņłśĒĢśĻ│Ā ļé┤ļČĆļĪ£ ĒÖĢņé░ĒĢśņŚ¼ ņłśņåīĒÖöļ¼╝ņØä ņäØņČ£ĒĢ£ļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņłśņåī ņןņ×ģņØĆ ņŗżņĀ£ ņĢĢļĀźĻ┤ĆņØś ņāüĒÖ®ņØä Ļ│ĀļĀżĒĢśņŚ¼ ņĀäĒĢ┤ ļ░®ļ▓Ģņ£╝ļĪ£ Ēæ£ļ®┤ņŚÉ ņłśņåīĒÖöļ¼╝ņØä ĒśĢņä▒ņŗ£Ēé©ļŗż. ņØ┤ Ļ│╝ņĀĢņØĆ 85 ┬░CņØś ņłśņÜ®ņĢĪņŚÉņä£ ņØ┤ļŻ©ņ¢┤ņ¦ĆĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņåīļź╝ ņ×¼ļŻī ļé┤ļČĆļĪ£ ņČ®ļČäĒ׳ ĒÖĢņé░ņŗ£Ēé¼ ņłś ņŚåļŗż. ņĢĢļĀźĻ┤Ć ņ×¼ļŻī ļé┤ļČĆļĪ£ ņłśņåīļź╝ ĒÖĢņé░ņŗ£ĒéżļŖö ļ░®ļ▓ĢņØĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ļź╝ ĒåĄĒĢśņŚ¼ Ēæ£ļ®┤ņØś ņłśņåīļź╝ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś ļé┤ļČĆļĪ£ ĒÖĢņé░ņŗ£Ēé©ļŗż [6].
Zr-2.5%Nb ĒĢ®ĻĖł ņĢĢļĀźĻ┤ĆņØĆ ļæÉĻ╗śĻ░Ć 4.3 mm ņĀĢļÅäņØ┤ļ»ĆļĪ£ ╬▒-ZrņŚÉņä£ņØś ĒÖĢņé░ ņåŹļÅäļź╝ Ļ│ĀļĀżĒĢśļ®┤ 350 ┬░CņŚÉņä£ ņĢĮ 13ņŗ£Ļ░äņØ┤ļ®┤ ņłśņåī ļåŹļÅäņØś ĻĘĀņ¦łĒÖöĻ░Ć ņÖäļŻīļÉśļŖö Ļ▓āņ£╝ļĪ£ Ļ│äņé░ļÉ£ļŗż. ĻĘĖļ¤╝ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņØ┤ļ│┤ļŗż 20ļ░░ ņĀĢļÅäņØś ĻĖ┤ ņŗ£Ļ░äņØä ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņśĆļŗż. ņØ┤ ņØ┤ņ£ĀļŖö ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņżæ Ēæ£ļ®┤ņØś ņé░ĒÖöļź╝ ļ░®ņ¦ĆĒĢśĻ│Ā ņłśņåī ņןņ×ģ Ļ│╝ņĀĢņŚÉņä£ ņŗ£ĒÄĖņØś Ēæ£ļ®┤ņŚÉ ĒśĢņä▒ļÉ£ ņłśņåīĒÖöļ¼╝ņØ┤ ņל ņ£Āņ¦ĆļÉĀ ņłś ņ׳ļÅäļĪØ Pyrex ļśÉļŖö Quartz ņ¦äĻ│Ą tubing ņåŹņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäļŖö Ēæ£ 2ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ 300-550 ┬░CņŚÉņä£ ņŗżņŗ£ĒĢśņśĆļŗż. ĻĘĖļ¤¼ļéś ņŗżņĀ£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņŗ£ĒÄĖņØś ņś©ļÅäļŖö ņĀäĻĖ░ļĪ£ņØś ņś©ļÅäļ│┤ļŗż ņĢĮĻ░ä ļé«ņØä ņłś ņ׳ļŗż.
ĻĘĀņ¦łĒÖö ņ▓śļ”¼ Ļ│╝ņĀĢņŚÉņä£ Ēæ£ļ®┤ņØś ņłśņåīļŖö ļé┤ļČĆļĪ£ ĒÖĢņé░ĒĢ£ļŗż. ņłśņåī ĒÖĢņé░ņØĆ ĻĖ░ņ¦ĆņØś Ļ▓░ņĀĢļ”ĮĻ│ä, ╬▒-Zr, ╬▓-ZrņØä ĒåĄĒĢśņŚ¼ ņØ┤ļŻ©ņ¢┤ņ¦äļŗż [2,3]. ņłśņåī ĒÖĢņé░ Ļ▓ĮļĪ£ ņżæņŚÉņä£ ņłśņåīņØś ĒÖĢņé░ ņåŹļÅäļŖö ņ×ģĻ│ä ĒÖĢņé░ņØ┤ Ļ░Ćņן ļ╣Āļź┤Ļ│Ā, BCC ĻĄ¼ņĪ░ņØś ╬▓-ZrņØä ĒåĄĒĢ£ ĒÖĢņé░, HCP Ļ▓░ņĀĢ ĻĄ¼ņĪ░ļź╝ Ļ░Ćņ¦ä ╬▒-ZrņØä ņł£ņ£╝ļĪ£ ļŖÉļĀżņ¦ł Ļ▓āņØ┤ļŗż. ņØ┤ ņØ┤ņ£ĀļŖö ņ×ģĻ│äĻ░Ć Ļ░Ćņן ņŚ┤ļ”░ ĻĄ¼ņĪ░ļź╝ Ļ░Ćņ¦ĆĻ│Ā ņ׳Ļ│Ā, BCCņØĖ ╬▓-ZrņØĆ ņĪ░ļ░ĆĒĢ£ HCP ĻĄ¼ņĪ░ņØś ╬▒-Zrļ│┤ļŗż ĒÖĢņé░ņØ┤ ļŹö ņÜ®ņØ┤ĒĢśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż [14]. ņØ┤ Ļ│╝ņĀĢņŚÉņä£ ņŗżņĀ£ ņłśņåī ĒÖĢņé░ņØĆ ņ×ģĻ│ä ĒÖĢņé░Ļ│╝ Ļ▓®ņ×É ĒÖĢņé░ņØś ĒÅēĒ¢ē (parallel) Ļ│╝ņĀĢņØ┤ļ»ĆļĪ£ ņ×ģĻ│ä ĒÖĢņé░ Ļ│╝ņĀĢņŚÉ ņØśĒĢ┤ ņ¦Ćļ░░ļÉĀ Ļ▓āņØ┤ļŗż.
ĻĘĀņ¦łĒÖö ņ▓śļ”¼ņŚÉ ņØśĒĢśņŚ¼ Ēæ£ļ®┤ņØś ņłśņåīĻ░Ć ĻĖ░ņ¦Ć ļé┤ļČĆļĪ£ ņØ┤ļÅÖĒĢśņŚ¼ Ļ│ĀņÜ® ĒĢ£ļÅäņŚÉ ļÅäļŗ¼Ē¢łņØä ļĢī ņłśņåīļŖö ņ¢┤ļööņŚÉ ņ¢┤ļ¢╗Ļ▓ī ļ░░ņ╣śļÉśļŖöĻ░Ć ĒĢśļŖö Ļ▓āņØ┤ ļāēĻ░ü Ļ│╝ņĀĢņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ Ļ│╝ņĀĢņŚÉ Ēü░ ņśüĒ¢źņØä ļ»Ėņ╣£ļŗż. ņłśņåī Ļ│ĀņÜ®ļÅä(terminal solid solubility, TSS)ļŖö Ļ▓░ņĀĢ ĻĄ¼ņĪ░ ņāü Ļ│ĄĻĘ╣ņØś Ēü¼ĻĖ░Ļ░Ć ļŹö Ēü░ HCP Ļ▓░ņĀĢņØś ╬▒-ZrņŚÉņä£ BCC ĻĄ¼ņĪ░ņØś ╬▓ ņāüļ│┤ļŗż ļŹö Ēü┤ Ļ▓āņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ļīĆļČĆļČäņØś ņłśņåīļŖö ╬▒-ZrņŚÉ ļ©Ėļ¼╝ Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
ņłśņåī Ļ│ĀņÜ®ļÅäļŖö ņś©ļÅäĻ░Ć ļé«ņĢäņ¦Ćļ®┤ ļé«ņĢäņ¦ĆĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņåīĒÖöļ¼╝ņØĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņØ┤Ēøä ļāēĻ░ü Ļ│╝ņĀĢņŚÉņä£ ņäØņČ£ĒĢśĻ▓ī ļÉ£ļŗż. ņłśņåīĒÖöļ¼╝ņØś ĒśĢņāüņØĆ ļāēĻ░ü ņåŹļÅäņŚÉ ļö░ļØ╝ ļŗ¼ļØ╝ņ¦ĆļŖöļŹ░ ņä£ļףĒĢśļ®┤ Ēü░ ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ĒĢśĻ│Ā ĻĖēļףĒĢśļ®┤ ņ×æņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ĒĢ£ļŗż [13]. ĻĖēļףĒĢśļ®┤ ņłśņåīņØś ĒÖĢņé░ņŚÉ ĒĢäņÜöĒĢ£ ņČ®ļČäĒĢ£ ņŗ£Ļ░äņØä ņĀ£Ļ│ĄĒĢśņ¦Ć ļ¬╗ĒĢśļ»ĆļĪ£ ņ×æņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ļÉśļŖö Ļ▓āņØĆ ļŗ╣ņŚ░ĒĢśļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņŗ£ĒÄĖņØĆ Pyrex tubing ņåŹņŚÉ ļōĀ ņāüĒā£ļĪ£ Ļ│ĄĻĖ░ ņżæņŚÉņä£ ļāēĻ░üļÉśņŚłļŗż. ņØ┤ Ļ│╝ņĀĢņØĆ ņ¦äĻ│ĄņØ┤ļØ╝ļŖö ĒŖ╣ņä▒ ļĢīļ¼ĖņŚÉ ļģĖļāē(furnace cooling)Ļ│╝ ņ£Āņé¼ĒĢśĻ▓ī ļāēĻ░üļÉśņŚłņØä Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ņŗ£ĒÄĖņØś ļāēĻ░ü ņåŹļÅäļŖö ĻĘĖļ”╝ 2ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ ĒīÉņāüņØś ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ĒĢ£ Ļ▓āņ£╝ļĪ£ļČĆĒä░ ņä£ļףļÉśņŚłļŗżļŖö Ļ▓āņØä ņ£ĀņČöĒĢĀ ņłś ņ׳ļŗż.
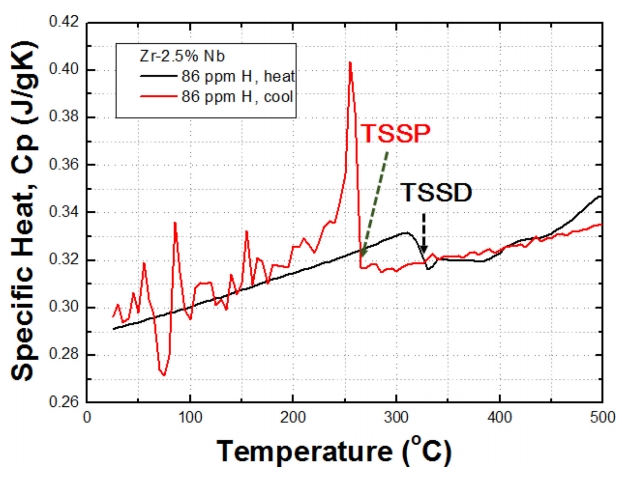
ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉņä£ ļāēĻ░üĒĢĀ ļĢī ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ņØä ņŗ£ņ×æĒĢśļŖö ņś©ļÅäļŖö ņłśņåī ļåŹļÅäņŚÉ ļö░ļØ╝ ļŗ¼ļØ╝ņ¦äļŗż. ĻĘĖļ”╝ 16ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ DSC ļČäņäØņ£╝ļĪ£ ļ╣äņŚ┤ņØä ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ņŚÉ ļö░ļź┤ļ®┤ 86 ppmņØś ņłśņåīļź╝ ĒĢ©ņ£ĀĒĢ£ ņŗ£ĒÄĖņŚÉņä£ ņłśņåīĒÖöļ¼╝ņØĆ Ļ░ĆņŚ┤ĒĢĀ ļĢī 324 ┬░CņŚÉņä£ ņÜ®ĒĢ┤ļÉśĻ│Ā ļāēĻ░üļÉĀ ļĢīļŖö 265 ┬░CņĀĢļÅäņŚÉņä£ ņäØņČ£ļÉśĻĖ░ ņŗ£ņ×æĒĢ£ļŗż. ņ”ē, ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ĒĢśĻĖ░ ņŗ£ņ×æĒĢśļŖö TSSP ņś©ļÅäļŖö Kearns ļō▒[6]ņØ┤ ╬▒-ZrņŚÉ ļīĆĒĢ£ ņłśņåī Ļ│ĀņÜ®ļÅäļź╝ ņĖĪņĀĢĒĢśņŚ¼ ņĀ£ņŗ£ĒĢ£ TSSD ņś©ļÅäļ│┤ļŗż ņĢĮ 60 ┬░C ņĀĢļÅä ļé«ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņé¼ņÜ®ĒĢ£ ņŗ£ĒÄĖ ņżæņŚÉņä£ 350 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśņŚ¼ ņłśņåī ļåŹļÅäĻ░Ć 86 ppmņØĖ ņŗ£ĒÄĖņØĆ ņłśņåīĻ░Ć ņÜ®ĒĢ┤ļÉ£ ņāüĒā£ņŚÉņä£ ņłśņåīļŖö 265 ┬░CĻ╣īņ¦Ć Ļ│ĀņÜ®ļÉśņ¢┤ ņ׳ļŗżĻ░Ć ņäØņČ£ĒĢśĻĖ░ ņŗ£ņ×æĒĢ£ļŗż. ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ĒĢśĻĖ░ ņĀä ņłśņåīļŖö ĒÖĢņé░ Ļ│äņłśĻ░Ć Ēü░ ╬▓-ZrņŚÉņä£ ĒÖĢņé░ Ļ│äņłśĻ░Ć ņ×æņØĆ ╬▒-Zrņ£╝ļĪ£ ņØ┤ļÅÖĒĢśĻĖ░ļŖö ņÜ®ņØ┤ĒĢśņ¦Ć ņĢŖņ£╝ļ»ĆļĪ£ ņłśņåīļŖö ╬▒-Zr ļ░Å ╬▓ ņāüņØś Ļ│äļ®┤ņŚÉ ļ©Ėļ¼╝ Ļ░ĆļŖźņä▒ņØ┤ Ēü¼ļŗż. ņ£äņŚÉņä£ ņ¢ĖĻĖēĒĢ£ ļ░öņÖĆ Ļ░ÖņØ┤ ņĢĢļĀźĻ┤Ć ņ×¼ļŻīļŖö as-received ņĪ░Ļ▒┤ņŚÉņä£ ╬▒-ZrĻ│╝ ╬▓-ZrļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳Ļ│Ā, ╬▓-ZrņØĆ ╬▒-ZrņØś Ļ│äļ®┤ņŚÉ ņŚ░ņåŹņĀüņ£╝ļĪ£ ļČäĒżĒĢ£ļŗż [2,3]. ļīĆļČĆļČäņØś ņäØņČ£ Ļ│╝ņĀĢņØĆ ļČłĻĘĀņØ╝ (heterogeneous) ĒĢĄņāØņä▒ņŚÉ ņØśĒĢ┤ ņØ╝ņ¢┤ļéśļ»ĆļĪ£ ņłśņåīĒÖöļ¼╝ņØĆ ņäØņČ£ļÅä ╬▒/╬▓ ņāü Ļ│äļ®┤ņŚÉņä£ņØś ļČłĻĘĀņØ╝ ĒĢĄņāØņä▒ņŚÉ ņØśĒĢ┤ ņ¦Ćļ░░ļÉ£ļŗż.
ĻĘĖļ”╝ 15ņŚÉ ļéśĒāĆļéĖ ļ░öņÖĆ Ļ░ÖņØ┤ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļØ╝ ļ»ĖņäĖņĪ░ņ¦üņØ┤ ļ│ĆĒÖöļÉ£ļŗżļŖö Ļ▓āņØĆ ĒÖĢņØĖļÉśņŚłļŗż. ļ»ĖņäĖņĪ░ņ¦üņØ┤ as-received ņĪ░Ļ▒┤ņŚÉ Ļ░Ćņן ņ£Āņé¼ĒĢ£ 350 ┬░C ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņŗ£ĒÄĖņØĆ ╬▒-ZrĻ│╝ ╬▓-Zr Ļ│äļ®┤ņØ┤ ņŚ░ņåŹņĀüņØĖ ĻĄ¼ņĪ░ņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ņØĆ ņØ┤ Ļ│äļ®┤ņØä ļö░ļØ╝ ņÜ®ņØ┤ĒĢśĻ▓ī ĒĢĄņāØņä▒ ļÉśĻ│Ā ņØ┤ļōżņØĆ ņä£ļĪ£ ņŚ░Ļ▓░ļÉśļ®┤ņä£ ņä▒ņןĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ 50╬╝mĻ╣īņ¦Ć ĻĖ┤ ņłśņåīĒÖöļ¼╝ņØ┤ ĒśĢņä▒ļÉśļŖö Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ņ”ē, 350 ┬░C ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņŗ£ĒÄĖņØĆ ĒĢĄņāØņä▒ ņ£äņ╣śļ│┤ļŗżļŖö ņłśņåīĒÖöļ¼╝ ņä▒ņןņŚÉ ņØśĒĢ┤ ņ¦Ćļ░░ļÉśļŖö Ļ│╝ņĀĢņØ┤ļØ╝Ļ│Ā ņäżļ¬ģĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ”╝ 16ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ DSC ļČäņäØ Ļ▓░Ļ│╝ļŖö ņłśņåīĒÖöļ¼╝ ņäØņČ£ņØĆ 265 ┬░C ņØ┤ĒĢśņŚÉņä£ ņØ╝ņ¢┤ļéśļŖö ļ░śņØæņØ┤ĻĖ░ ļĢīļ¼ĖņØ┤ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņłśņåīĒÖöļ¼╝ ņäØņČ£ Ļ▒░ļÅÖņØĆ 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ņŗ£ĒÄĖĻ│╝ 475 ┬░C ņØ┤ņāüņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓āņØä ļö░ļĪ£ ņäżļ¬ģĒĢśĻ│Āņ×É ĒĢśņśĆļŗż. ņØ┤ ņØ┤ņ£ĀļŖö ĻĘĖļ”╝ 15ņŚÉ ļ│┤ņØĖ XRD Ļ▓░Ļ│╝ļŖö 350 ┬░CņŚÉņä£ 500ņŗ£Ļ░ä ņŚ┤ņ▓śļ”¼ĒĢśļ®┤ Žē ņāüņØ┤ ļéśĒāĆļéśĻ│Ā 400 ┬░CņŚÉņä£ 240ņŗ£Ļ░ä ņ£Āņ¦ĆĒĢśļ®┤ ╬▓-Zr ņāüņØĆ ņÖäņĀäĒ׳ ļČäĒĢ┤ļÉśĻ│Ā ╬▓-Nb ņāüņØ┤ ĒśĢņä▒ļÉśļŖö Ļ▓āņØä ļ│┤ņØĖļŗż. ļśÉĒĢ£ Zr-2.5%Nb ņĢĢļĀźĻ┤ĆņØś ņĀ£ņĪ░ Ļ│╝ņĀĢņŚÉņä£ ņØæļĀź ņĀ£ņ▓ś ņ▓śļ”¼ļŖö 400 ┬░C 24ņŗ£Ļ░ä ņĪ░Ļ▒┤ņŚÉņä£ ņŗżņŗ£ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ ņŗ£ĒÄĖņØĆ ļ»ĖņäĖņĪ░ņ¦üņØś ļ│ĆĒÖöĻ░Ć Ļ░Ćņן ņĀüĻĖ░ ļĢīļ¼ĖņØ┤ļŗż.
400 ┬░C ņØ┤ĒĢśņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓ĮņÜ░, ĻĘĖļ”╝ 6ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ ņłśņåī ļåŹļÅäĻ░Ć 14 ppmņŚÉņä£ 28 ppmņ£╝ļĪ£ ņ”ØĻ░ĆĒĢĀ ļĢī ņłśņåīĒÖöļ¼╝ņØś Ļ░£ņłśļŖö ņĢĮ 300% ņ”ØĻ░ĆĒĢśĻ│Ā ĻĖĖņØ┤ļŖö ņĢĮ 60% ņĀĢļÅä ļŖśņ¢┤ļé£ļŗż. ĻĘĖļ¤¼ļéś ļåŹļÅäĻ░Ć 86 ppmņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśņŚ¼ļÅä ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö ņĢĮ 10% Ļ░ÉņåīĒĢśĻ│Ā ĻĖĖņØ┤ļŖö 300% ņĀĢļÅä ņ”ØĻ░ĆĒĢśļŖö Ļ▓āņØä ņĢī ņłś ņ׳ļŗż. ņ”ē, ņłśņåī ļåŹļÅäĻ░Ć 14 ppmņŚÉņä£ 28 ppmņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśļ®┤ ņłśņåīĒÖöļ¼╝ņØś ņłśĻ░Ć ĻĖēĻ▓®Ē׳ ņ”ØĻ░ĆĒĢśĻ│Ā, ĻĘĖ ņØ┤ņāüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśļ®┤ ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö ņ”ØĻ░ĆĒĢśņ¦Ć ņĢŖĻ│Ā ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤Ļ░Ć ĻĖĖņ¢┤ņ¦äļŗż. ņØ┤ Ļ│╝ņĀĢņØĆ ņłśņåī ļåŹļÅäĻ░Ć ņ”ØĻ░ĆĒĢĀ ļĢī ņłśņåīĒÖöļ¼╝ņØś ņä▒ņןņØĆ ņ¦¦ņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņä£ļĪ£ ņŚ░Ļ▓░ļÉśļ®┤ņä£ ņä▒ņןĒĢśĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ļ│┤ņØĖļŗż.
╬▓ ņāüņØś ļČäĒĢ┤Ļ░Ć ņØ╝ņ¢┤ļéśļŖö 400 ┬░C ņØ┤ņāüņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ ņłśņåīĒÖöļ¼╝ ņäØņČ£ ĒŖ╣ņä▒ņØ┤ ļŗ¼ļØ╝ņ¦äļŗż. ņłśņåī ļåŹļÅäĻ░Ć ņ£Āņé¼ĒĢ£ 81-86 ppmņØś ņŗ£ĒÄĖļōżņØĆ 350, 400, 475 ┬░CņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢ£ Ļ▓āņØ┤ļŗż. ņØ┤ ņŗ£ĒÄĖņØś ņłśņåīĒÖöļ¼╝ ņäØņČ£ ĒŖ╣ņä▒ņØĆ ĻĘĖļ”╝ 9ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņŚÉ ļö░ļØ╝ ņ¦üņäĀņĀüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśĻ│Ā, ĻĖĖņØ┤/ļæÉĻ╗śņØś ļ╣äņ£©ņØĆ Ļ░ÉņåīĒĢ£ļŗż. ĻĘĖļ”╝ 12-14ņŚÉ ļ│┤ņØĖ ļ░öņÖĆ Ļ░ÖņØ┤ 400, 475, 550 ┬░CņŚÉņä£ņØś TEM ļ»ĖņäĖņĪ░ņ¦üņØś ļ│ĆĒÖöņŚÉ ņØśĒĢ┤ ņל ļÆĘļ░øņ╣©ļÉ£ļŗż. 400 ┬░CņØ┤ņāüņŚÉņä£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ĒĢśļ®┤ ╬▓ ņāüņØĆ ļČäĒĢ┤ļÉśņ¢┤ ļČłņŚ░ņåŹņĀüņØĖ ĒśĢņāüņ£╝ļĪ£ ļ░öļĆīļ»ĆļĪ£ ĒĢĄņāØņä▒ņØ┤ ņÜ®ņØ┤ĒĢ£ ņ£äņ╣śĻ░Ć ņ”ØĻ░ĆĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤Ļ░Ć ņ¦¦ņĢäņ¦ĆĻ│Ā ņłśļŖö ļŖśņ¢┤ļéśļŖö Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö Ļ┤æĒĢÖĒśäļ»ĖĻ▓Įņ£╝ļĪ£ ņłśņåīĒÖöļ¼╝ņØä Ļ┤Ćņ░░ĒĢśņŚ¼ Ļ▒░ņŗ£ņĀüņØĖ ņłśņåīĒÖöļ¼╝ ņäØņČ£ Ļ▒░ļÅÖņØä ņŚ░ĻĄ¼ĒĢ£ Ļ▓āņØ┤ļŗż. ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ĒśĢĒā£ļź╝ ļģ╝ņØśĒĢĀ ļĢī Ļ▒░ņŗ£ņĀüņØĖ ļ®┤Ļ│╝ ļ»Ėņŗ£ņĀüņØĖ ļ®┤ņØä Ļ│ĀļĀżĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż. Ļ▒░ņŗ£ņĀüņ£╝ļĪ£ ņłśņåīĒÖöļ¼╝ņØĆ ņĢĢļĀźĻ┤ĆņØś ĻĖĖņØ┤-ĒÜĪ ļ®┤ņŚÉ ĒÅēĒ¢ēĒĢ£ ĒīÉņāüņ£╝ļĪ£ ņäØņČ£ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż. ĻĘĖļ¤¼ļéś ļ»Ėņŗ£ņĀüņ£╝ļĪ£ļŖö ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ļ®┤(habit plane)ņŚÉ ņäØņČ£ĒĢ£ ņłśņåīĒÖöļ¼╝ņØ┤ ņŚ░Ļ▓░ļÉśņ¢┤ Ļ▒░ņŗ£ņĀüņ£╝ļĪ£ļŖö Ēü░ ĒīÉ ĒśĢĒā£ļĪ£ ļ│┤ņØ┤ļŖö Ļ▓āņØ╝ ņłśļÅä ņ׳ļŗż [15].
ņŗżņĀ£ ņĢĢļĀźĻ┤ĆņŚÉņä£ ņØ╝ņ¢┤ļéśļŖö ņłśņåī ņ¦ĆņŚ░ ĻĘĀņŚ┤ (delayed hydride cracking, DHC) ĒśäņāüņØĆ ĻĘĀņŚ┤ņØ┤ļéś ļģĖņ╣śĻ░Ć ņĪ┤ņ×¼ĒĢśļŖö ņāüĒÖ®ņŚÉņä£ ņØ╝ņ¢┤ļé£ļŗż. Ļ▓░ĒĢ©ņŚÉ ņØśĒĢ┤ ņØæļĀźņØ┤ ņ¦æņżæļÉśĻ▒░ļéś ņØæļĀźņØ┤ Ļ░ĆĒĢ┤ņ¦ä ņāüĒā£ņŚÉņä£ļŖö ņØæļĀźņŚÉ ņłśņ¦üĒĢ£ ļ░®Ē¢źņ£╝ļĪ£ Ļ▒░ņŗ£ņĀüņØĖ ņłśņåīĒÖöļ¼╝ņØ┤ ņäØņČ£ļÉśĻ│Ā ĒīīĻ┤┤ļÉśļŖö Ļ│╝ņĀĢņØä ļ░śļ│ĄĒĢ£ļŗż [16]. ĻĘĖļ¤¼ļéś ļ│Ė ņŚ░ĻĄ¼ņŚÉ ņé¼ņÜ®ĒĢ£ ņŗ£ĒÄĖļōżņØĆ ņØæļĀźņØä ļ░øņ¦Ć ņĢŖļŖö ņāüĒā£ņŚÉņä£ņØś ņäØņČ£ Ļ▒░ļÅÖņØä ļČäņäØĒĢ£ Ļ▓āņØ┤ļŗż. ĻĘĖļ¤╝ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ Ļ▒░ņŗ£ņĀüņØĖ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ĒŖ╣ņä▒ņØä ņĀĢļ¤ēņĀüņ£╝ļĪ£ ņŚ░ĻĄ¼ĒĢ£ Ļ▓āņØĆ ņĄ£ņ┤łņØ┤ļ®░, ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņØś ņłśņåīĒÖöļ¼╝ ņäØņČ£ņØś Ļ▒░ļÅÖņØä ņĀĢļ¤ēņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢśļŖö ņĀäĻĖ░ļź╝ ļ¦łļĀ©Ē¢łļŗżļŖö ņĖĪļ®┤ņŚÉņä£ ņØśļ»Ėņ׳ļŗż.
5. Ļ▓░ ļĪĀ
Zr-2.5%Nb ĒĢ®ĻĖł ņĢĢļĀźĻ┤Ć ņ×¼ļŻīņŚÉņä£ 14-144 ppmņØś ņłśņåī ļåŹļÅäņÖĆ 300-550 ┬░CņŚÉņä£ņØś ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅä ļ│ĆĒÖöņŚÉ ļö░ļźĖ Ļ▒░ņŗ£ņĀüņØĖ ņłśņåīĒÖöļ¼╝ņØś ņäØņČ£ ĒŖ╣ņä▒ņØä MATLAB imageļĪ£ ņĀĢļ¤ē ļČäņäØĒĢ£ Ļ▓░Ļ│╝ ļŗżņØīĻ│╝ Ļ░ÖņØĆ Ļ▓░ļĪĀņØä ņ¢╗ņØä ņłś ņ׳ņŚłļŗż.
1. ņłśņåīĒÖöļ¼╝ ļ®┤ņĀü ļ╣äņ£©(ļČäņ£©)ņØĆ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņÖĆ Ļ┤ĆĻ│ä ņŚåņØ┤ ņłśņåī ļåŹļÅäņŚÉ ļö░ļØ╝ Ļ▒░ņØś ņ¦üņäĀņĀüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢ£ļŗż.
2. 400 ┬░C ņØ┤ĒĢśņŚÉņä£ ņłśņåī ļåŹļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļźĖ ņłśņåīĒÖöļ¼╝ņØś ĻĖĖņØ┤ ņä▒ņןņØĆ ņ¦¦ņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņä£ļĪ£ ņŚ░Ļ▓░ļÉśļŖö Ļ│╝ņĀĢņØä ĒåĄĒĢ┤ ņØ╝ņ¢┤ļé£ļŗż.
3. ņłśņåī ļåŹļÅäĻ░Ć 81-86 ppmņ£╝ļĪ£ ņ£Āņé¼ĒĢ£ Ļ▓ĮņÜ░ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäņØś ņ”ØĻ░ĆņŚÉ ļö░ļØ╝ ņäØņČ£ ņłśņåīĒÖöļ¼╝ņØś ņłśļŖö ņ”ØĻ░ĆĒĢśĻ│Ā ĻĖĖņØ┤/ļæÉĻ╗śņØś ļ╣äņ£©ņØĆ Ļ░ÉņåīĒĢśļŖöļŹ░, ņØ┤Ļ▓āņØĆ ņłśņåīĒÖöļ¼╝ņØ┤ ņä£ļĪ£ ņŚ░Ļ▓░ļÉśĻĖ░ ņ¢┤ļĀĄĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
4. 475 ┬░C ņØ┤ņāüņ£╝ļĪ£ ĻĘĀņ¦łĒÖö ņ▓śļ”¼ ņś©ļÅäĻ░Ć ņ”ØĻ░ĆĒĢĀ ļĢī ļéśĒāĆļéśļŖö ņłśņåīĒÖöļ¼╝ ņäØņČ£ Ļ▒░ļÅÖņØś ļ│ĆĒÖöļŖö ╬▒-ZrĻ│╝ ╬▓ ņāü ņĪ░ņ¦ü ļ│ĆĒÖöņŚÉ ļö░ļźĖ ĒĢĄņāØņä▒Ļ│╝ ņä▒ņן Ļ▒░ļÅÖņØś ļ│ĆĒÖö ļĢīļ¼ĖņØ┤ļŗż.